��Ŀ����
����Ŀ��������Ϊ����������Դ֮һ���Ѿ��ܵ�����������ձ��ע����Ĵ洢������Ӧ�õ���Ҫƿ����Ŀǰ�����û������о�����Ҫ���ⷽ��������λ�⻯�ﴢ�⡢̼�ʲ��ϴ��⡢�Ͻ��⡢��ײ��ϴ���ȡ�
��ش�����������
��1��������( NH3BH3)��һ��DZ�ڵĴ�����ϣ���������Ԫ��״������(HB=NH)3ͨ��3CH4+2(HB=NH)3+6H2O=3CO2+6H3BNH3�Ƶ���
��B��C��N��O��һ�������ɴ�С��˳��Ϊ_____________��CH4��H2O��CO2�����ɴ�С��˳��Ϊ_________________��
��1��(HB=NH)3��������______����������(HB=NH)3��Ϊ�ȵ�����ķ���Ϊ________(�����ʽ)��
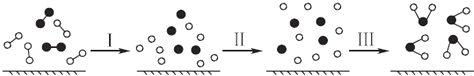
����Ӧǰ��̼ԭ�ӵ��ӻ�������ͷֱ�Ϊ__________��____________��
���������ڸ������ͷ�������ɵ�������������������ƽ��ʯ�Ľṹ�����۵�Ƚ��ʯ�ͣ�ԭ����___________________________��
��2��һ�ִ���Ͻ���������(La)������侧���ṹ��ͼ��ʾ��

��Ni �Ļ�̬ԭ�Ӻ�������Ų�ʽΪ_______________��
���þ���Ļ�ѧʽΪ_______________��
���þ�����ڲ����п�϶����ÿ�������Ŀ�϶�д���6����ԭ�ӱȽ��ȶ�����֪��a=m pm��c=n pm����״�����������ܶ�Ϊ��g��cm-3�������ӵ�������ֵΪNA������������ǰ��������仯����ô�����ϵĴ�������Ϊ______________�� (��������=![]() )
)
���𰸡� N>O>C>B CO2>CH4>H2O 12 C6H6 sp3 sp B��N���ļ�������C��C���ģ�����С��C��C����(ָ����������ܹ�ϵ������) 1s22s22p63s23p63d84s2��[Ar]3d84s2 LaNi5 ![]() ����
���� ��
��
����������1�������һ�����ܵĹ��ɡ����ǵĴ�С����ѧ����Ŀ���жϡ��ӻ����͵��жϣ������۷е�ߵ͵��жϣ���ͬ���ڴ������ҵ�һ����������IIA>IIIA��VA>VIA����˵�һ�����ܴ�С˳����N>O>C>B��CH4�ļ�����109��28�䣬H2O�ļ�����105�㣬CO2�ļ�����180�㣬˳����CO2>CH4>H2O���ڳɼ�ԭ�Ӽ�ֻ���γ�һ���Ҽ���(HB=NH)3Ϊ��Ԫ��״��������1��(HB=NH)3�к��ЦҼ�����Ϊ12�������ݵȵ�����ĸ����Լ�(HB=NH)3Ϊ��Ԫ��״������Ƴ��ȵ�����ķ���ΪC6H6���۷�ӦǰCΪsp3�ӻ�����Ӧ��̼ԭ��Ϊsp�ӻ�����������������������ƽ��ʯ�Ľṹ����������������Ϊԭ�Ӿ��壬�Ƚ�ԭ�Ӿ����۷е�ͨ�����������ܿ��ǣ�B��N���ļ�������C��C���ģ�����С��C��C�������������������۷е���ڽ��ʯ����2����������Ų�ʽ�������ļ��㣬��Niλ�ڵ�������VIII�壬28��Ԫ�أ�Ni�ĺ�������Ų�ʽΪ1s22s22p63s23p63d84s2��[Ar]3d84s2����Laλ�ڶ��㣬����Ϊ8��1/8=1��Niλ�����Ϻ����ģ�����Ϊ8��1/2��1=5����ѧʽΪLaNi5��������������Ϊ![]() g�����������Ϊ(m��10��10��m��10��10��n��10��10��sin60��)cm3��������������ܶ�Ϊ
g�����������Ϊ(m��10��10��m��10��10��n��10��10��sin60��)cm3��������������ܶ�Ϊ g/cm3����˴�����ϹʵĴ�������Ϊ
g/cm3����˴�����ϹʵĴ�������Ϊ![]() ����
����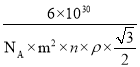 ����
����
�㾦��������ѵ��Ǵ��������ļ��㣬��Ȼ��Ŀ�и���ѧ��������������Ĺ�ʽ����ѧ���Դ�����������ܶ����ⲻ�������м��㣬��ʵ������������ܶȾ���������������������������뾧������ı�ֵ����ƽʱ��ϰ�����ܶȵļ�����һ���ģ�ֻ�����������������������������
�����͡�������
��������
12
����Ŀ��G��һ���������ϵ����ɷ�֮һ����ṹ�к���������Ԫ����G �ĺϳ�·������ͼ��ʾ(���ֲ���ͷ�Ӧ��������ȥ)��

��֪����RCH=CH2+CH2=CHR'![]() CH2=CH2+RCH=CHR'��
CH2=CH2+RCH=CHR'��
��B�ĺ˴Ź�������ͼ��ʾ��������6�ֲ�ͬ��������ԭ����
��D��F��ͬϵ�
��ش�����������
��1������ϵͳ��������(CH3)2C=CH2������Ϊ_____________��
��2��A��B��Ӧ�������漰�ķ�Ӧ���ͷֱ�Ϊ_______________��_________________��
��3������E�Ļ�ѧ����ʽΪ______________________________��
��4��G�Ľṹ��ʽΪ_________________��
��5��д��һ��ͬʱ��������������F��ͬ���칹��Ľṹ��ʽ��_________________��
����FeCl3��Һ������ɫ��Ӧ����������������ȡ��������C=O�������ܷ���ˮ�ⷴӦ�����˴Ź���������4��塣
��6��ģ���ɱ���ϩ�ϳ�F�ķ�����д���ɱ�ϩ��ȡa-�ǻ�����(![]() ) �ĺϳ�·����____________________________��
) �ĺϳ�·����____________________________��
���𰸡� 2-��-1-��ϩ(��2-����ϩ�������ϩ) ȡ����Ӧ �ӳɷ�Ӧ 
 ����
���� ��
�� ![]() (��
(��![]() )
) 
�������������л�����ƶϺͺϳɣ���1������ϩ��������ԭ��(CH3)2C=CH2������Ϊ2-��-1-��ϩ(��2-����ϩ�������ϩ)����2��������Ϣ�٣��Լ�A��Ӧ�IJ�����A�Ľṹ��ʽΪ ���Ա�A�Ͳ���Ľṹ��ʽ��A����
���Ա�A�Ͳ���Ľṹ��ʽ��A���� ��Ӧ����Ϊȡ����Ӧ���Աȷ���ʽ��
��Ӧ����Ϊȡ����Ӧ���Աȷ���ʽ�� ��B����һ��HCl�������ķ�Ӧ�Ǽӳɷ�Ӧ��B�Ľṹ��ʽ������
��B����һ��HCl�������ķ�Ӧ�Ǽӳɷ�Ӧ��B�Ľṹ��ʽ������ ����
���� ����ΪB�ĺ˴Ź���������6�ֲ�ͬ��������ԭ�ӣ����B�Ľṹ��ʽΪ
����ΪB�ĺ˴Ź���������6�ֲ�ͬ��������ԭ�ӣ����B�Ľṹ��ʽΪ ��B����C����±������ˮ�ⷴӦ����C�Ľṹ��ʽΪ
��B����C����±������ˮ�ⷴӦ����C�Ľṹ��ʽΪ ��C����D����������Ӧ����D�Ľṹ��ʽΪ
��C����D����������Ӧ����D�Ľṹ��ʽΪ ������ϩ��HO��Br�����ӳɷ�Ӧ��E�Ľṹ��ʽΪ
������ϩ��HO��Br�����ӳɷ�Ӧ��E�Ľṹ��ʽΪ ��
�� ��ǰ�߱�������
��ǰ�߱������� �����߱�������
�����߱������� �����߲�������Ϣ��E�Ľṹ��ʽΪ
�����߲�������Ϣ��E�Ľṹ��ʽΪ ��E�IJ�����
��E�IJ����� ��F�Ľṹ��ʽΪ
��F�Ľṹ��ʽΪ ����3�����ݣ�2���ķ���������E�ķ�Ӧ����ʽΪ
����3�����ݣ�2���ķ���������E�ķ�Ӧ����ʽΪ ����4��G��������Ԫ��������G������������Ӧ����G�Ľṹ��ʽΪ/span>
����4��G��������Ԫ��������G������������Ӧ����G�Ľṹ��ʽΪ/span> ����
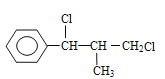
���� �� ����5����FeCl3������ɫ��Ӧ��˵�����з��ǻ���������������ȡ��������C=O�����ܷ���ˮ�⣬˵�������������˴Ź���������4����ԭ��������ȡ�������ڶ�λ�������������Ľṹ��ʽΪ
�� ����5����FeCl3������ɫ��Ӧ��˵�����з��ǻ���������������ȡ��������C=O�����ܷ���ˮ�⣬˵�������������˴Ź���������4����ԭ��������ȡ�������ڶ�λ�������������Ľṹ��ʽΪ![]() (��
(��![]() ) ����6����ϩ����HO��Br�����ӳɷ�Ӧ��Ȼ�������������ˮ�⣬���ϳ�·����
) ����6����ϩ����HO��Br�����ӳɷ�Ӧ��Ȼ�������������ˮ�⣬���ϳ�·���� ��
��

 �Ͻ�ƽСѧ��������ϵ�д�
�Ͻ�ƽСѧ��������ϵ�д� �Ƹ������������ϵ�д�
�Ƹ������������ϵ�д�