题目内容
【题目】下列说法中错误的是()
A. 甲烷与乙烯共lmol,完全燃烧后生成2molH2O
B. 光照下,异丁烷与Cl2发生取代反应生成的一氯代物有2种
C. 乙烯可以用作生产食品包装材料的原料
D. 乙酸分子中含有碳氧双键,所以它能使溴水褪色
【答案】D
【解析】A、每摩尔甲烷或者乙烯都含有4摩尔氢原子,根据原子守恒可知完全燃烧后生成的H2O为2mol,选项A正确;B、光照下,异丁烷分子中有2种不同的H原子,故其一氯代物有2种,选项B正确;C、乙烯可以制成聚乙烯,用于食品包装,选项C正确;D、乙酸分子中含有碳氧双键,但由于与羟基相连接,形成新的官能团羧基,所以它不能使溴水褪色,选项D错误。答案选D。

 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案【题目】“一碳化学”是指以含一个碳原子的化合物(如:CO2、CO、CH4、CH3OH等)为初始反应物,合成一系列重要的化工原料和燃料的化学。
(1)以CO2和NH3为原料合成尿素是利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应I:2NH3(g)+CO2(g)=NH2COONH4(s)△H1
反应II:NH2COONH4(s)=CO(NH2)2(s)+H2O(g) △H2=+72.49kJ/mol
总反应:2NH3(g)+CO2(g)==CO(NH2)2(s)+H2O(g) △H3=-86.98kJ/mol
请回答下列问题:
①反应I的△H1=______ kJ/mol
②反应II一般在_________(填“高温”或“低温”)情况下有利于该反应的进行。
③一定温度下,在体积为固定的密闭容器中按计量比进行反应I,下列能说明反应达到了平衡状态的是__________(填序号)。
A.混合气体的平均相对分子质量不再变化 B.容器内气体总压强不再变化
C.2V正(NH3)=V逆(CO2) D.容器内混合气体的密度不再变化
④环境为真空时,在一敞开容器(非密闭容器)中加入NH2COONH4固体,足够长时间后,反应是否建立平衡状态? ___________(填“是”或“否”)
(2)将CO2和H2充入一定体积的密闭容器中,在两种温度下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)。测得CH3OH的物质的量随时间的变化如下图。
CH3OH(g)+H2O(g)。测得CH3OH的物质的量随时间的变化如下图。
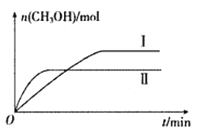
①曲线I.II对应的平衡常数大小关系为KI_______KII(填“ >”、“<”或“=”)。
②一定温度下,在容积相同且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
容器 | 甲 | 乙 |
反应物投入量 | 1molCO2、3molH2 | amolCO2、bmolH2 cmol CH3OH(g)、cmolH2O(g)(a、b、c均不为零) |
若甲容器平衡后气体的压强为开始的0.8倍,则甲容器平衡混合气体中CH3OH(g)的体积分数为_______,要使平衡后乙容器与甲容器中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,乙容器中c的取值范围为________。
(3)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系如下图,乙酸的生成速率主要取决于温度影响的范围是________________。

【题目】下图是元素周期表的一部分
A | |||||||||||||||||
B | C | D | E | F | |||||||||||||
H | I | J | K | ||||||||||||||
L | M | O |
(1)元素L的价电子排布图为__________,元素M的原子结构示意图为________,位于元素周期表五个区域中的_______区。上述元素中电负性最强的是_______(用元素符号表示),C、D、E、F第一电离能的大小顺序为____________(用元素符号表示)。
(2)D的氢化物和J氢化物沸点较高的是______(填化学式),稳定性更强的是______(填化学式)。
(3)某些不同族元素的性质也有一定的相似性,如上表中元素I与元素B的单质有相似的性质。写出元素单质B与NaOH溶液反应的离子方程式___________________________。
(4)A、E、H、J四种元素的原子半径由大到小的排列顺序为___________________;E、F、H、K四种元素简单离子的半径由大到小的排列顺序为________________用元素符号表示)。
(5)能证明元素K比元素J的非金属性强的事实是______________(填序号)。
A.常温下K单质的密度小于J单质的密度
B.K元素的气态氢化物比J元素的气态氢化物更稳定
C.K单质与氢气反应的程度比J单质与氢气反应的程度更剧烈
D.K元素的氧化物对应的水化物酸性强于J元素的氧化物对应的水化物


