��Ŀ����
����Ŀ��1000mLij����Һ�г�����0.2molL��1��Na+�⣬�����ܺ������������е�һ�ֻ���֣�
������ | K+��NH4+��Fe3+��Ba2+ |
������ | Cl����Br����CO32����HCO3����SO32����SO42�� |
�ֽ�������ʵ������������Լ�����������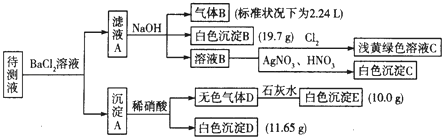
��1��д�����ɰ�ɫ����B�����ӷ���ʽ�� ��
��2������ɫ����D�ǵ�һ���壺 �ٽ������ӵ����ʵ���Ũ�������±��У�һ�������ڵ��0��������ȷ�������������
������ | Cl�� | Br�� | CO32�� | HCO3�� | SO32�� | SO42�� |
Ũ��/molL��1 |
���ж�ԭ��Һ��K+�Ƿ���ڣ������ڣ��������ʵ���Ũ�ȵ���Сֵ���������ڣ���˵�����ɣ� ��
��3������ɫ����D�ǻ�����壬����Һ��һ�����е��������� ��
���𰸡�
��1��HCO3��+Ba2++OH��=BaCO3��+H2O
��2�����ڣ�K+������СŨ��Ϊ0.1mol/L
��3��CO32����HCO3����SO32��
���������⣺����Һ���Ȼ�����Һ��Ӧ�õ�����A������Һ�п��ܺ���CO32����SO32����SO42�� �� ������м���ϡ�����������壬���в��ֳ������ܽ⣬����Һ�д���CO32�� �� ���ܴ���SO32����SO42���е����ֻ�һ�֣��������ӹ���֪����Һ�в�����Ba2+�� ��ҺA����Ba2+ �� ���������NaOH��Һ�õ�����B����ɫ����B������Һ��һ������NH4+��HCO3�� �� һ��������Fe3+ �� ����BΪNH3 �� ��ɫ����BΪBaCO3 �� ��ҺB��ͨ����������dz����ɫ��Һ����Һ��һ��û��Br�� �� ��ҺB�м�����������������Һ�õ���ɫ����C��CΪAgCl��˵����ҺB�к���Cl�� �� ���ڼ����Ȼ�����Һ������ȷ��ԭ��Һ���Ƿ���Cl������1��������������֪����ɫ����BΪ̼�ᱵ������HCO3����Ba2+��OH����Ӧ���ɣ���Ӧ���ӷ���ʽΪ��HCO3��+Ba2++OH��=BaCO3��+H2O��
�ʴ�Ϊ��HCO3��+Ba2++OH��=BaCO3��+H2O����2����������������֪������ȷ��ԭ��Һ���Ƿ���Cl�� �� ��Һ��һ��û��Br�� ��
����ɫ����D�ǵ�һ���壬��DΪCO2 �� EΪCaCO3 �� ��Һ�к���CO32�� �� ��ɫ����Dֻ��ΪBaSO4 �� ��Һ��һ��û��SO32�� �� һ������SO42�� ��
B��̼�ᱵ�������ʵ���= ![]() =0.1mol����n��HCO3����=0.1mol����c��HCO3����=
=0.1mol����n��HCO3����=0.1mol����c��HCO3����= ![]() =0.1mol/L��
=0.1mol/L��
E��̼��ƣ������ʵ���= ![]() =0.1mol����n��CO32����=0.1mol����c��CO32����=
=0.1mol����n��CO32����=0.1mol����c��CO32����= ![]() =0.1mol/L��
=0.1mol/L��
D�����ᱵ�������ʵ���= ![]() =0.05mol����n��SO42����=0.05mol����c��SO42����=
=0.05mol����n��SO42����=0.05mol����c��SO42����= ![]() =0.05mol/L��
=0.05mol/L��
�ʴ�Ϊ��
������ | Cl�� | Br�� | CO32�� | HCO3�� | SO32�� | SO42�� |
Ũ��/molL��1 | �� | 0 | 0.1 | 0.1 | 0 | 0.05 |
��n��NH4+��=n��NH3��= ![]() =0.1mol����c��NH4+��=0.1mol/L����Һ��c��Na+��=0.2mol/L��c��HCO3����=0.1mol/L��c��CO32����=0.1mol/L��c��SO42����=0.05mol/L����λ���Ϊ�����=1��0.1mol/L+1��0.2mol/L=0.3mol/L����λ����ڸ����=1��0.1mol/L+2��0.1mol/L+2��0.05mol/L=0.4mol/L����λ���Ϊ����ɣ���λ����ڸ���ɣ���һ������K+ �� ����Һ��û��Cl�� �� K+����Ũ����С�����ݵ���غ��֪��c��K+����СŨ��=0.4mol/L��0.3mol��L=0.1mol/L��
=0.1mol����c��NH4+��=0.1mol/L����Һ��c��Na+��=0.2mol/L��c��HCO3����=0.1mol/L��c��CO32����=0.1mol/L��c��SO42����=0.05mol/L����λ���Ϊ�����=1��0.1mol/L+1��0.2mol/L=0.3mol/L����λ����ڸ����=1��0.1mol/L+2��0.1mol/L+2��0.05mol/L=0.4mol/L����λ���Ϊ����ɣ���λ����ڸ���ɣ���һ������K+ �� ����Һ��û��Cl�� �� K+����Ũ����С�����ݵ���غ��֪��c��K+����СŨ��=0.4mol/L��0.3mol��L=0.1mol/L��
�ʴ�Ϊ�����ڣ�K+������СŨ��Ϊ0.1mol/L����3����������������֪����Һ��һ������CO32����HCO3�� �� ����ȷ��ԭ��Һ���Ƿ���Cl�� �� ��Һ��һ��û��Br�� ��
����ɫ����D�ǻ�����壬ֻ��ΪCO2��NO������壬��ɫ����Dֻ��ΪBaSO4 �� ��Һ��һ������SO32�� �� ����ȷ���Ƿ���SO42�� �� ����Һ��һ�����е���������CO32����HCO3����SO32�� ��
�ʴ�Ϊ��CO32����HCO3����SO32�� ��
��1������Һ���Ȼ�����Һ��Ӧ�õ�����A������Һ�п��ܺ���CO32����SO32����SO42�� �� ������м���ϡ�����������壬���в��ֳ������ܽ⣬����Һ�д���CO32�� �� ���ܴ���SO32����SO42���е����ֻ�һ�֣��������ӹ���֪����Һ�в�����Ba2+��
��ҺA����Ba2+ �� ���������NaOH��Һ�õ�����B����ɫ����B������Һ��һ������NH4+��HCO3�� �� һ��������Fe3+ �� ����BΪNH3 �� ��ɫ����BΪBaCO3 �� ��ҺB��ͨ����������dz����ɫ��Һ����Һ��һ��û��Br�� �� ��ҺB�м�����������������Һ�õ���ɫ����C��CΪAgCl��˵����ҺB�к���Cl�� �� ���ڼ����Ȼ�����Һ������ȷ��ԭ��Һ���Ƿ���Cl������2������ɫ����D�ǵ�һ���壬��DΪCO2 �� EΪCaCO3 �� ��Һ�к���CO32�� �� ��ɫ����Dֻ��ΪBaSO4 �� ��Һ��һ��û��SO32�� �� һ������SO42�� �� ����B��̼�ᱵ����E��̼��ƣ������ᱵ�����ʵ��������������غ��������ӵ�Ũ�ȣ�
���ݵ���غ��ж��Ƿ��м����ӣ�����Һ����K+ �� ����Һ��û��Cl�� �� K+����Ũ����С�����ݵ���غ���㣻��3����Һ��һ������CO32����HCO3�� �� ����ȷ��ԭ��Һ���Ƿ���Cl�� �� ��Һ��һ��û��Br�� �� ����ɫ����D�ǻ�����壬ֻ��ΪCO2��NO������壬��ɫ����Dֻ��ΪBaSO4 �� ��Һ��һ������SO32�� �� ����ȷ���Ƿ���SO42�� ��

����Ŀ��������Ԫ��A��B��C��D�����й����ʻ�ṹ��Ϣ�����ʾ��
Ԫ�� | A | B | C | D |
�й����ʻ�ṹ��Ϣ | ���γ�+7�۵Ļ����� | ��̬ԭ�Ӻ���s�ܼ��ϵĵ�������p�ܼ��ϵĵ�������2�� | ��Ԫ���γɵĵ���ͨ��������ͬ�������壬����һ�ֵ��ʷֲ��ڸ߿գ�������ֹ������������ | ͨ����������γɶ����������ȶ���˫ԭ���ӷ��� |
��1��Bλ��Ԫ�����ڱ��е����ڵ��壬Ԫ��B��Ԫ��C��ȣ��縺�Խ�С������дԪ�����ƣ���������BC2������B�ĵ��ʾ���������ͬһ���ͻ�ͬ���ͣ���
��2��д��Ԫ��C�ĺ���10�����ӵ�һ�ֺ��ط��� �� B��һ���⻯��B2H2�����ЦҼ���м�����Ŀ֮��Ϊ ��
��3��C��D������ɶ�����ʽ�Ļ��������D2C5�ܹ�ˮ��Ӧ��������X��д������X��ϡ��Һ�������Fe��Ӧ�����ӷ���ʽ��
��4��A�����{��������Ϊ��ɫҺ�壬9.15g��������������ˮ��ϣ��õ�һ��ϡ��Һ�����ų�QKJ�������÷�Ӧ���Ȼ�ѧ��Ӧ����ʽΪ ��
