题目内容
9.下列说法正确的是( )| A. | 标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA | |
| B. | 1molCl2与足量Fe反应,转移的电子数为3NA | |
| C. | 常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3NA | |
| D. | 在H2O2+Cl2=2HCl+O2反应中,每生成32g 氧气,转移2NA个电子 |
分析 A、氯气和氢氧化钠的反应为歧化反应;
B、氯气和铁反应后,氯元素变为-1价;
C、常温常压下,气体摩尔体积大于22.4L/mol;
D、H2O2+Cl2=2HCl+O2反应,转移2mol电子,生成1mol氧气.
解答 解:A、标况下,2.24L氯气的物质的量为0.1mol,而氯气和氢氧化钠的反应为歧化反应,当1mol氯气反应时转移1mol电子,则0.1mol氯气转移0.1mol电子即0.1NA个,故A错误;
B、氯气和铁反应后,氯元素变为-1价,故1mol氯气反应后转移2mol电子即2NA个,故B错误;
C、常温常压下,气体摩尔体积大于22.4L/mol,则33.6L氯气的物质的量小于1.5mol,当和27g铝即1mol铝反应时,铝过量,故转移的电子的物质的量小于3mol即小于3NA个,故C错误;
D、H2O2+Cl2=2HCl+O2反应,转移2mol电子即2NA个时生成1mol氧气,质量为32g,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
19.下列实验操作正确的是( )
| A. |  滴加液体 | B. |  取用固体 | C. |  测溶液pH | D. |  过滤 |
20.水的摩尔质量和N的相对原子质量分别是( )
| A. | 18和15 | B. | 18g和14 | C. | 18g/mol和14 | D. | 18g/mol和15 |
14.二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用.工业上可利用煤的气化产物(水煤气)合成二甲醚.
(1)煤的气化的主要化学反应方程式为:C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2.
(2)利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g)═CH3OH(g);△H=-90.8kJ•mol-1
②2CH3OH(g)═CH3OCH3(g)+H2O(g);△H=-23.5kJ•mol-1
③CO(g)+H2O(g)═CO2(g)+H2(g);△H=-41.3kJ•mol-1
总反应:3H2(g)+3CO(g)═CH3OCH3(g)+CO2 (g)的△H=-246.4kJ•mol-1;一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是c、e(填字母代号).
a.高温高压 b.加入催化剂 c.减少CO2的浓度
d.增加CO的浓度 e.分离出二甲醚
(3)已知反应②2CH3OH(g)═CH3OCH3(g)+H2O(g)某温度下的平衡常数为400.
此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
①比较此时正、逆反应速率的大小:v正> v逆 (填“>”、“<”或“=”).
②若加入CH3OH后,经10min反应达到平衡,此时c(CH3OH)=0.04mol•L-1;该时间内反应速率v(CH3OH)=0.16mol/(L•min).
(1)煤的气化的主要化学反应方程式为:C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2.
(2)利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g)═CH3OH(g);△H=-90.8kJ•mol-1
②2CH3OH(g)═CH3OCH3(g)+H2O(g);△H=-23.5kJ•mol-1
③CO(g)+H2O(g)═CO2(g)+H2(g);△H=-41.3kJ•mol-1
总反应:3H2(g)+3CO(g)═CH3OCH3(g)+CO2 (g)的△H=-246.4kJ•mol-1;一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是c、e(填字母代号).
a.高温高压 b.加入催化剂 c.减少CO2的浓度
d.增加CO的浓度 e.分离出二甲醚
(3)已知反应②2CH3OH(g)═CH3OCH3(g)+H2O(g)某温度下的平衡常数为400.
此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol•L-1) | 0.44 | 0.6 | 0.6 |
②若加入CH3OH后,经10min反应达到平衡,此时c(CH3OH)=0.04mol•L-1;该时间内反应速率v(CH3OH)=0.16mol/(L•min).
1.如图所示,△H1=-393.5kJ•mol-1,△H2=-395.4kJ•mol-1,下列说法或表示式正确的是( )
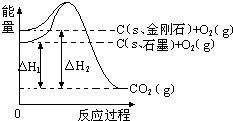

| A. | C(s、石墨)═C(s、金刚石)△H=+1.9kJ•mol-1 | |
| B. | 石墨和金刚石的转化是物理变化 | |
| C. | 石墨的稳定性强于金刚石 | |
| D. | 1mol石墨的总键能比1mol金刚石的总键能小1.9kJ |
19.实验室制备硅酸的反应为Na2SiO3+2HCl═2NaCl+H2SiO3↓,该反应属于( )
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |

