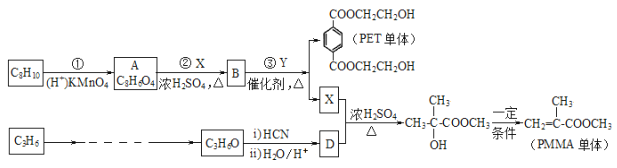
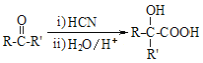��Ŀ����
����Ŀ������ֻ�ܱ�����A��B��A������һ�������ƶ��Ļ�����ʹ�����ڱ��ֺ�ѹ��B�����ܱ��ֺ��ݡ���ʼʱ�������������зֱ��������ʵ���SO3���壬��ʹA��B�ݻ����(��ͼ��ʾ)������400�������·�����Ӧ:2SO2��O2![]() 2SO3��������������ȷ���ǣ� ��
2SO3��������������ȷ���ǣ� ��
A. �ﵽƽ������Ҫ��ʱ��:A��������
B. �ﵽƽ��ʱ:B������SO3��ת���ʸ���
C. �ﵽƽ��ʱ:A������SO2�����ʵ�������
D. �ﵽƽ������������зֱ�ͨ������ĺ�����A������SO3�������������
���𰸡�C
��������A����ʼʱ�������������зֱ��������ʵ���SO3���壬��Ӧ����������ʵ�������ķ����ƶ���A������һ�������ƶ��Ļ�����ʹ�����ڱ��ֺ�ѹ��B�����ܱ��ֺ��ݣ���A��ѹǿС��B��ѹǿ��ѹǿԽ��Ӧ����Խ����B�ﵽƽ������Ҫ��ʱ��̣�A����B��ѹǿ����ƽ��������SO3�ķ����ƶ���B������SO3��ת����С��B����C��A��ѹǿС��������SO2�����ɣ���ﵽƽ��ʱA������SO2�����ʵ������࣬C��ȷ��D���ﵽƽ������������зֱ�ͨ������ĺ�����A��������ѹǿ�仯���������������ƽ��������SO2�ķ����ƶ���A������SO3�����������С��B������䣬������ƽ��û��Ӱ�죬B������SO3������������䣬D����ѡC��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ��������(DME)����Ϊ��21���͵����ȼ�������ɺϳ����Ʊ������ѵ���Ҫԭ�����£�
��CO(g)+2H2(g)![]() CH3OH(g)��H1=-90.7 kJ��mol-1
CH3OH(g)��H1=-90.7 kJ��mol-1
��2CH3OH(g)![]() CH3OCH3(g)+H2O(g)��H2=-23.5kJ��mol-1
CH3OCH3(g)+H2O(g)��H2=-23.5kJ��mol-1
��CO(g)+H2O(g)![]() CO2(g)+H2(g)��H3=-41.2 kJ��mol-1
CO2(g)+H2(g)��H3=-41.2 kJ��mol-1
�ش��������⣺
��1����Ӧ3H2(g)+3CO(g)![]() CH3OCH3(g)+CO2(g)����H=_____________kJ��mol-1��
CH3OCH3(g)+CO2(g)����H=_____________kJ��mol-1��
��2���ڲ�ͬ�¶��°�����ͬ���ʵ���Ͷ�Ϸ�����Ӧ�٣����CO��ƽ��ת������ѹǿ�Ĺ�ϵ��ͼ��ʾ������˵����ȷ����_____________��
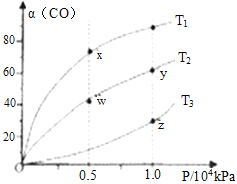
A����Ӧ�¶ȣ�T1>T2 B������Ӧ���ʣ�����(y)=����(w)
C����������ܶȣ���(x)>��(w) D���������ƽ��Ħ��������M(y)<M(z)
E���÷�Ӧ����S<0����H<0���������ڽϵ��¶����Է�����
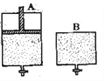
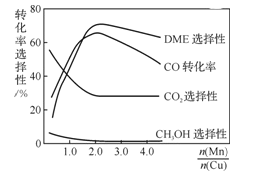
��3������һ�����͵Ĵ���(��Ҫ�ɷ���Cu-Mn�ĺϽ�)������CO��H2�Ʊ�������(DME)����ͼ�ش�����;������![]() ԼΪ_____________ʱ�������ڶ����ѵĺϳɡ�
ԼΪ_____________ʱ�������ڶ����ѵĺϳɡ�
��4������ʱ�����ѷ����ֽⷴӦ��CH3OCH3![]() CH4+CO+H2��Ѹ�ٽ�����������һ��504���ij����յ�ƿ�У��ڲ�ͬʱ��t�ⶨƿ��ѹǿP�����±���
CH4+CO+H2��Ѹ�ٽ�����������һ��504���ij����յ�ƿ�У��ڲ�ͬʱ��t�ⶨƿ��ѹǿP�����±���
t/min | 0 | 10 | 20 | 30 | 40 | 50 |
P��/kPa | 50.0 | 78.0 | 92.0 | 99.0 | 100 | 100 |
���÷�Ӧ��ƽ�ⳣ������ʽΪKp=_____________��
���÷�Ӧ��ƽ�ⳣ��Kp=_____________��(����λ��ijһ���ʵ�ƽ���ѹ=��ѹ�����ʵ�������)
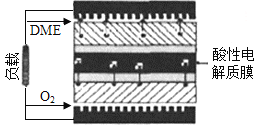
��5��һ���Զ�������Ϊȼ�ϵ�ȼ�ϵ�صĹ���ԭ����ͼ��ʾ�����为���ĵ缫��ӦʽΪ_______________���õ�ص����������ѹΪ1.20V�����������ܶ�E=_____________(��ʽ���㡣�����ܶ�=����������/ȼ��������1kW��h=3.6��106J�������ڳ���F=96500C��mol-1)��
����Ŀ������Ŀ��X��Y��Z��W��R��M����Ԫ�أ�λ��Ԫ�����ڱ���ǰ�����ڣ����ǵĺ˵�����������������Ϣ���£�
Ԫ�� | �����Ϣ |
X | �䵥��Ϊ���壬�����缫���� |
Y | ԭ�Ӻ�����6�ֲ�ͬ�˶�״̬�ĵ��� |
Z | �ǽ���Ԫ�أ���̬ԭ�ӵ�s����ĵ���������p����ĵ���������ͬ |
W | ����Ԫ�أ���Zԭ�ӵļ۵�������ͬ |
R | �۲�����Ų�Ϊ3d64s2 |
M | ��B�壬�䵥�ʳ��������� |
��ش���������(����ʱ��X��Y��Z��W��R��M������Ӧ��Ԫ�ط��ű�ʾ)��
��1��X�ĵ�����Z�ĵ��ʷ�Ӧ�IJ���Ϊ_____________��(�ѧʽ)��
��2��Z��W��ȣ���һ�����ܽϴ����_____________��M2+�ĺ�������Ų�ʽΪ_____________��
��3��M2Z���۵��M2W��_____________(����������������)�������ԭ��______________________��
��4��Y��Z�γɵĻ�����YZ2��VSEPRģ��Ϊ__________������Yԭ�����ӻ��������Ϊ____________;N3-��YZ2��Ϊ�ȵ����壬��N3-�ĽṹʽΪ_____________��
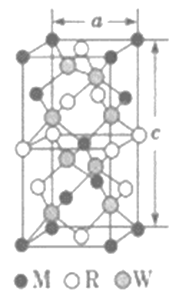
��5��MRW2�ľ�����ͼ��ʾ����������a=0.524nm,c=1.032nm;MRW2�ľ�����ÿ��Mԭ����_________��Wԭ�������������ܶ���=________g��cm-3(ֻҪ������ʽ�����ؼ������ֵ��NA=6.02��1023mol-1)��