��Ŀ����
3��þ�ڶ�����̼����ȼ�գ��Ʊ�þ�����ã���ô�����ڶ�����̼��ȼ����ij�о���ѧϰС�����������װ�ý���̽����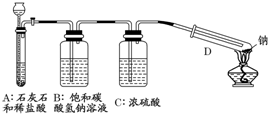
��1��д��þ�ڶ�����̼��ȼ�յĻ�ѧ��Ӧ����ʽ2Mg+CO2 $\frac{\underline{\;��ȼ\;}}{\;}$2MgO+C��
��2����װ���б���̼��������Һ�������dz�ȥCO2�л��е�HCl��Ũ����������Ǹ���CO2���壮
��3���þƾ������Թ�D�ײ����ȣ����ڳ���������̼������Թ�����ҵ�ȼ�գ����������İ��̣��Թܵײ��к�ɫ�������ɣ��Թ���ȴ���Թܱ��ϸ���һ���ɫ���ʣ����Թ��м�ˮ����ɫ�����ܽ���ˮ����ɫ���ʲ��ܣ����ˣ��õ��������Һ������Һ�мӳ���ʯ��ˮ����Һ����ǣ��ٵ���ϡ���ᣬ��Һ�������ݳ��֣����Թܱ��ϸ��ŵİ�ɫ������Na2CO3������ֽ�ϵĺ�ɫ���������������գ���ɫ������ȼ�գ���ú�ɫ������C��̼������д�����������̼��Ӧ�Ļ�ѧ����ʽ��4Na+3CO2$\frac{\underline{\;\;��\;\;}}{\;}$2Na2CO3+C��
���� ̽�����ܷ��ڶ�����̼��ȼ��ʵ�����̣�������ȡ�����Ķ�����̼��Aװ����ȡ������̼���ٳ�����ȡ�л��е��Ȼ������塢ˮ��Bװ�ó��Ȼ�������ʱ������������������Һ����Ϊ�������ƻ�Ͷ�����̼��Ӧ��Cװ�ó�ˮʱ��Ũ��������������ڵ�ȼDװ���еľƾ���ǰ�������ȥϵͳ���ڵĿ�������ֹ��������е�������Ӧ��ͨ���������������̽��ʵ��ɵó����������̼��Ӧ������̼���ƺ�̼��
��1��þ���������̼�����û���Ӧ����̼������þ��
��2��ʯ��ʯ�����ᷴӦ��ȡ������̼�������ӷ���װ��B�������dz�ȥ������̼�е��Ȼ������壻
��3���þƾ������Թ�D�ײ����ȣ����ڳ���������̼������Թ�����ҵ�ȼ�գ����������İ����ܽ���ˮ�ӳ���ʯ��ˮ����Һ����ǣ��ٵ���ϡ���ᣬ��Һ�������ݳ���ΪNa2CO3����ɫ���ʲ���ΪC��
��� �⣺��1��þ���������̼�����û���Ӧ������̼������þ����ӦΪ2Mg+CO2 $\frac{\underline{\;��ȼ\;}}{\;}$2MgO+C��
�ʴ�Ϊ��2Mg+CO2 $\frac{\underline{\;��ȼ\;}}{\;}$2MgO+C��
��2��ʯ��ʯ�����ᷴӦ��ȡ������̼�������ӷ����ƵõĶ�����̼�л����Ȼ��⣬װ��B�������dz�ȥ�Ȼ������壻�ڳ��Ȼ�������ʱ������������������Һ����Ϊ�������ƻ�Ͷ�����̼��Ӧ��������̼��̼�������в��ܣ����ñ���̼�������������Ȼ��⣬Ũ���������ˮ�ԣ�������Ũ�����������������ˮ��
�ʴ�Ϊ����ȥCO2�л��е�HCl������CO2���壻
��3����ɫ���ʵ���ϡ���ᣬ��Һ�������ݳ��֣�ӦΪNa2CO3������ֽ�ϵĺ�ɫ���ʸ����ȼ����ȼ�ղ�����ɫ��ζ����ʹ����ʯ��ˮ����ǣ��������еĺ�ɫ������̼���漰��ӦΪ4Na+3CO2$\frac{\underline{\;\;��\;\;}}{\;}$2Na2CO3+C��
�ʴ�Ϊ��Na2CO3��C��̼����4Na+3CO2$\frac{\underline{\;\;��\;\;}}{\;}$2Na2CO3+C��
���� ���⿼��������ʵ�鷽������ƺ�̽���������ڻ���֪ʶ�Ŀ��飬ע�����ʵ��ԭ�������ʵ����ʣ�Ϊ������Ĺؼ�������ʱע�������Ϣ�ͷ�Ӧ����ע����ϸ���⣬��Ŀ�Ѷ��еȣ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�| A�� | ��״���£�22.4 L H2O�к��еķ�����ΪNA | |
| B�� | 1 mol•L-1 Na2CO3��Һ�к��е���������Ϊ2NA | |
| C�� | 28 g N2�к��е�ԭ����ΪNA | |
| D�� | 1 mol Mg������ϡ���ᷴӦ��ת�Ƶĵ�����Ϊ2NA |
 ̼�͵��Ƕ�ֲ�����ڵ���Ҫ���Ԫ�أ�������й����ŷŶ�����̼���������ЧӦ�������������ɹ⻯ѧ������Ŀǰ����Щ�ж��к�����Ĵ�����Ϊ��ѧ�о�����Ҫ���ݣ�
̼�͵��Ƕ�ֲ�����ڵ���Ҫ���Ԫ�أ�������й����ŷŶ�����̼���������ЧӦ�������������ɹ⻯ѧ������Ŀǰ����Щ�ж��к�����Ĵ�����Ϊ��ѧ�о�����Ҫ���ݣ����û���̿��ԭ��������������йط�ӦΪ��C��s��+2NO��g��?N2��g��+CO2��g����ij�о�С����һ���ݻ�������ܱ������������ݻ�Ϊ3L����������������Բ��ƣ��м���NO�������Ļ���̿���ں��£�T�棩�����·�Ӧ����ò�ͬʱ�䣨t��ʱ�����ʵ����ʵ�����n�������
| n/mol t/mol | NO | N2 | CO2 |
| 0 | 2.00 | 0 | 0 |
| 10 | 1.16 | 0.42 | 0.42 |
| 20 | 0.80 | 0.60 | 0.60 |
| 30 | 0.80 | 0.60 | 0.60 |
�ڸ��ݱ������ݣ�����T��ʱ�÷�Ӧ��ƽ�ⳣ��Ϊ0.56��������λС������
�����и������жϸ÷�Ӧ�ﵽƽ��״̬����CD
A��������ѹǿ���ֲ��� B.2v��NO����=v��N2����
C��������CO2������������� D�����������ܶȱ��ֲ���
��һ���¶��£�����NO����ʼŨ��������NO��ƽ��ת���ʲ��䣨����������䡱��С������
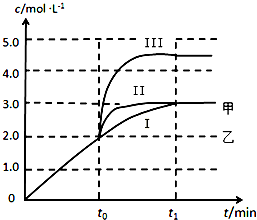
����3L�ݻ��ɱ���ܱ������з�����ӦH2��g��+CO2��g��?H2O��g��+CO��g����������c��CO����ʱ��t�仯������I��ͼ��ʾ������t0ʱ�ֱ�ı�һ������������I�������II������III��
�ٵ�����I�������IIʱ���ı�������Ǽ��������
�ڵ�����I�������IIIʱ���ı���������ı������ı仯���ֱ�������ѹǿ��ѹǿ��Ϊԭ����1.5��
| A�� | �ƾ�--��ȼƷ | B�� | Ũ����--��ʴƷ | ||
| C�� | �ռ�--�綾Ʒ | D�� | �����--ǿ������ |
| A�� | 2Na2O2+2H2O=4NaOH+O2�� | B�� | 2Al+2NaOH+2H2O=2NaAlO2+3H2�� | ||
| C�� | 2F2+2H2O=4HF+O2 | D�� | 4Fe��OH��2+O2+2H2O=4Fe��OH��3 |
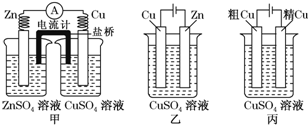
| A�� | ����ԭ��أ����ǵ��װ�� | |
| B�� | �ס���װ���У�п���Ͼ�����������Ӧ | |
| C�� | �ҡ���װ���У�����������������Ӧ���ܽ� | |
| D�� | �ҡ���װ���У�c��Cu2+���������� |
| A�� | Ca2+��Na+��CO2- | B�� | H+��Ca2+��HCO3- | C�� | K+��Na+��NO3-�� | D�� | NH4+��OH-��Cu2+ |