题目内容
5.设NA为阿伏加德罗常数的值,下列说法正确的是( )| A. | 常温常压下,16克O3中含有的原子数为NA | |
| B. | 标准状况下,22.4L液溴中含有的分子数为NA | |
| C. | 1molH2O中含有的原子个数为NA | |
| D. | 0.1mol/L硫酸铝溶液中含有硫酸根的个数为0.3NA |
分析 A、臭氧是由氧原子构成的;
B、标况下,溴为液体;
C、水分子由2个氢原子和1个氧原子构成;
D、溶液体积不明确.
解答 解:A、臭氧是由氧原子构成的,故16g臭氧中含有的氧原子的物质的量n=$\frac{16g}{16g/mol}$=1mol,即NA个,故A正确;
B、标况下,溴为液体,不能根据气体摩尔体积来计算,故B错误;
C、水分子由2个氢原子和1个氧原子构成,故1mol水中含3mol原子,故C错误;
D、溶液体积不明确,故溶液中的硫酸根的个数无法计算,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的计算,根据公式和物质的结构和状态来分析是解题的关键,难度不大.

练习册系列答案
相关题目
15.下列关于化学反应的描述中正确的是( )
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3kJ/mol,则含40.0gNaOH的稀溶液与醋酸完全中和,放出57.3kJ的热量 | |
| C. | CO(g)的燃烧热是283.0kJ/mol,则表示CO(g)的燃烧热的热方程式为2CO(g)+O2(g)=2CO2(g)△H=-283.0kJ/mol | |
| D. | 已知2C(s)+2O2(g)=2CO2(g)△H=akJ/mol,2C(s)+O2(g)=2CO(g)△H=bkJ/mol,则b>a |
20.下列各组物质按酸、碱、盐分类顺次排列的是( )
| A. | 硫酸、纯碱、胆矾 | B. | 硝酸、烧碱、食盐 | ||
| C. | 醋酸、乙醇、硫酸铵 | D. | 盐酸、熟石灰、苛性钠 |
10.下列说法错误的是( )
| A. | 氯气的摩尔质量是71 g/mol | |
| B. | 通过树状分类法可把硝酸和硫酸分入强酸,把纯碱分入正盐 | |
| C. | 酸性的雨水都是酸雨,酸雨的PH小于7 | |
| D. | 1mol CO2的质量是44 g |
14.能在水溶液中大量共存的一组离子是( )
| A. | Ba2+、K+、OH-、SO42- | B. | Fe3+、NO3-、Na+、OH- | ||
| C. | H+、Na+、Cl-、SO42- | D. | K+、SO42-、HCO3-、H+ |
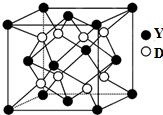 已知A、B、C、D、X、Y是原子序数依次增大的前20号元素,其中A~D的原子序数 是连号的,A的基态原子有3个不同的能级,各能级中的电子数相等;X和Y位于同一主族,
已知A、B、C、D、X、Y是原子序数依次增大的前20号元素,其中A~D的原子序数 是连号的,A的基态原子有3个不同的能级,各能级中的电子数相等;X和Y位于同一主族,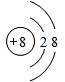 .
.