题目内容
【题目】固体粉末X中可能含有Fe、Fe2O3、K2SiO3、K2SO3、K[Al(OH)4]、MgCl2、K2CO3中的若干种。为确定该固体粉末的成分,现取X进行连续实验,实验过程及现象如下:
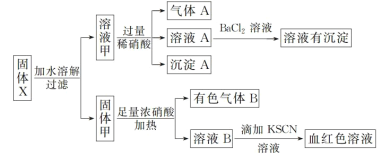
根据上述实验,以下说法正确的是( )
A.气体A一定只是NO
B.由于在溶液A中加入BaCl2溶液有沉淀产生,因此可以判断溶液甲中含有K2SO3
C.若向固体甲中加入足量浓盐酸,再加KSCN溶液,没有血红色,则证明原混合物中一定没有Fe2O3
D.溶液甲中一定含有K2SiO3,可能含有K[Al(OH)4]、MgCl2
【答案】B
【解析】
固体粉末X中Fe、Fe2O3不溶于水,加入浓硝酸,产生有色气体二氧化氮,则一定含有金属铁,得到的溶液B中含有硝酸铁,遇到硫氰化钾显示血红色,K2SiO3、K2SO3、K[Al(OH)4]、MgCl2、K2CO3能溶于水,向其中过量的稀硝酸,硅酸钾和H+反应得到硅酸沉淀,则原物质中一定含有K2SiO3,则一定不含有MgCl2,K2SO3被氧化为硫酸钾,会产生NO气体,K[Al(OH)4]和稀硝酸反应,先析出沉淀随后溶解,MgCl2不和硝酸反应,K2CO3可以和稀硝酸反应生成二氧化碳气体,溶液A中加入氯化钡,产生沉淀,则原物质中一定含有K2SO3,可能含有K[Al(OH)4]、K2CO3,则一定不含有MgCl2,据此回答判断。
固体粉末X中Fe、Fe2O3不溶于水,加入浓硝酸,产生有色气体二氧化氮,则一定含有金属铁,得到的溶液B中含有硝酸铁,遇到硫氰化钾显示血红色,K2SiO3、K2SO3、K[Al(OH)4]、MgCl2、K2CO3能溶于水,向其中过量的稀硝酸,硅酸钾和H+反应得到硅酸沉淀,则原物质中一定含有K2SiO3,则一定不含有MgCl2,K2SO3被氧化为硫酸钾,会产生NO气体,K[Al(OH)4]和稀硝酸反应,先析出沉淀随后溶解,MgCl2不和硝酸反应,K2CO3可以和稀硝酸反应生成二氧化碳气体,溶液A中加入氯化钡,产生沉淀,则原物质中一定含有K2SO3,可能含有K[Al(OH)4]、K2CO3,则一定不含有MgCl2;综上可知:原物质中一定含有:Fe、K2SiO3、K2SO3,可能含有:K[Al(OH)4]、K2CO3,Fe2O3;
A.气体A中含有NO,还可能含有CO2,故A错误;
B.溶液A中加入氯化钡,产生沉淀,则原物质中一定含有K2SO3,故B正确;
C.若向固体甲中加入足量浓盐酸,再加KSCN溶液,没有血红色,可能是Fe2O3和盐酸反应生成的铁离子和含有的金属铁之间反应转化为亚铁离子了,所以加KSCN溶液,没有血红色,不能证明原混合物中一定没有Fe2O3,故C错误;
D.溶液甲中一定含有K2SiO3,一定不含有MgCl2,可能含有K[Al(OH)4]、K2CO3,故D错误;
故答案选B。

 名校课堂系列答案
名校课堂系列答案