题目内容
2. 短周期元素Q、R、T、W在周期表中的位置如图所示,其中,T所处周期序数与主族序数相等,则下列说法正确的是( )
短周期元素Q、R、T、W在周期表中的位置如图所示,其中,T所处周期序数与主族序数相等,则下列说法正确的是( )| A. | 元素R的最高价氧化物对应的水化物是高沸点酸 | |
| B. | 元素T和W各自形成的简单离子都能促进水的电离 | |
| C. | 简单离子半径:W>T>R | |
| D. | 常温下,T的单质能完全溶于R的最高价氧化物的水化物的浓溶液中 |
分析 由短周期元素Q、R、T、W在元素周期表中的位置,可知Q、R处于第二周期,T、W处于第三周期,T所处的周期序数与主族序数相等,则T为Al,可推知Q为C元素、R为N元素、W为S元素,据此结合元素化合物的性质和元素周期律解答.
解答 解:由上述分析可知,Q为C,R为N,T为Al,W为S,
A.元素R的最高价氧化物对应的水化物为硝酸,为低沸点易挥发性酸,故A错误;
B.铝离子水解溶液显酸性,硫离子水解显碱性,所以元素T和W各自形成的简单离子都能促进水的电离,故B正确;
C.电子层越多,离子半径越大,电子层相同的离子中原子序数大的离子半径小,所以简单离子半径:W>R>T,故C错误;
D.常温下,Al在浓硫酸中会钝化,则Al在浓硫酸中不能完全溶解,故D错误;
故选B.
点评 本题考查位置、结构与性质,为高频考点,把握元素的位置、原子结构来推断元素为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识及规律性知识的应用,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.设NA表示阿伏加得罗常数,下列叙述正确的是( )
| A. | 标准状况下,1mol氦气所含的原子数为2NA | |
| B. | 1.8g NH4+离子中所含的电子数为1.1NA | |
| C. | 常温常压下,44g二氧化碳分子中所形成的共用电子对数为4NA | |
| D. | NA个氮分子和NA个氢分子的体积相同 |
13.已知一定温度下,2X(g)+Y(g) 2Z(g)反应每消耗1molY放出akJ的热量,现有甲、乙两容积相等且固定的密闭容器,在保持该温度恒定的条件下,向密闭容器甲中通入2molX和1molY,达到平衡状态时,放出热量bkJ;向密闭容器乙中通入1molX和0.5molY,达到平衡时,放出热量ckJ,且,则a、b、c的值或关系正确的是( )
2Z(g)反应每消耗1molY放出akJ的热量,现有甲、乙两容积相等且固定的密闭容器,在保持该温度恒定的条件下,向密闭容器甲中通入2molX和1molY,达到平衡状态时,放出热量bkJ;向密闭容器乙中通入1molX和0.5molY,达到平衡时,放出热量ckJ,且,则a、b、c的值或关系正确的是( )
 2Z(g)反应每消耗1molY放出akJ的热量,现有甲、乙两容积相等且固定的密闭容器,在保持该温度恒定的条件下,向密闭容器甲中通入2molX和1molY,达到平衡状态时,放出热量bkJ;向密闭容器乙中通入1molX和0.5molY,达到平衡时,放出热量ckJ,且,则a、b、c的值或关系正确的是( )
2Z(g)反应每消耗1molY放出akJ的热量,现有甲、乙两容积相等且固定的密闭容器,在保持该温度恒定的条件下,向密闭容器甲中通入2molX和1molY,达到平衡状态时,放出热量bkJ;向密闭容器乙中通入1molX和0.5molY,达到平衡时,放出热量ckJ,且,则a、b、c的值或关系正确的是( )| A. | 2b=c | B. | a=b | C. | a>2c | D. | 以上都不正确 |
10.已知有A、B、C、D、E五种短周期元素,其原子序数依次增大,A与B形成的共价化合物的水溶液呈碱性,C元素原子的最内层电子数是最外层电子数的2倍,D是同周期中单核离子半径最小的元素,E元素的最高正价与最低负价的代数和为6.下列叙述中错误的是( )
| A. | B元素的简单气态氢化物与E的氢化物化合,生成物的水溶液呈酸性 | |
| B. | B、C、E最高价氧化物对应的水化物溶液均能与D元素的氧化物反应 | |
| C. | 元素B、E分别与元素A构成的含有18个电子的分子中均含有非极性共价键 | |
| D. | 最高价氧化物对应水化物的碱性:C>D |
17.X、Y、Z、M、W、N六种元素的原子序数依次增大,其中X、Y、Z、M、W为五种短周期元素.X元素的某种核素无中子,W原子核外电子数是M原子最外层电子数的2倍,Y、Z、M、W在周期表中的相对位置如图所示,N是用量最多的金属元素.下列说法不正确的是( )
| Y | Z | M | |
| W |
| A. | 原子半径:W>Y>Z>M>X | |
| B. | N的一种氧化物可用作油漆和涂料 | |
| C. | 氢化物的沸点:Z大于M | |
| D. | 工业上制备W单质的方法为电解熔融的W的氧化物 |
8.下列有关实验操作错误的是( )
| A. | 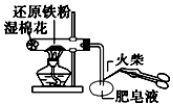 验铁粉与水蒸气反应产生的氢气 | |
| B. |  分离两种互溶但沸点相差较大的液体混合物 | |
| C. |  乙酸乙酯的制备演示实验 | |
| D. |  碳酸氢钠受热分解 |
5.下列各项实验操作与现象及结论或解释合理的是( )
| 选项 | 实验操作 | 现象 | 结论或解释 |
| A | 将稀盐酸滴入加有酚酞的Na2SiO3溶液中,边加边震荡, | 红色变浅并接近消失 | 有硅酸胶体生成 |
| B | 氯化钠晶体导电实验 | 不导电 | 晶体不存在离子 |
| C | AgI悬浊液中滴入Na2S溶液 | 固体变黑 | Ksp(Ag2S)>Ksp(AgI) |
| D | 测量H2CO3的电离常数 | Ka1>ka2 | H2CO3一级电离常数产生的H+对二级电离起抑制作用 |
| A. | A | B. | B | C. | C | D. | D |
9.M、N、Q、R为原子序数依次增大的短周期主族元素,N是形成有机物基本骨架的元素,M与N、Q可分别形成共价化合物S、T,且S、T分子中含相同的电子数.金属单质R在Q的单质中燃烧生成的化合物W可与T发生氧化还原反应.下列说法正确的是( )
| A. | 原子半径大小:M<N<Q<R | |
| B. | W中的阴阳离子个数比为1:1,属于离子化合物 | |
| C. | Q的某单质可作水的消毒剂,该单质在大气中含量越多,对人体越有益 | |
| D. | M和N、Q均能形成既含极性键又含非极性键的分子 |

 .
. +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2 .
.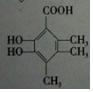 .
.