题目内容
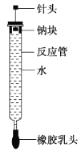
【题目】如图所示,当容器A中的反应开始后,若分别进行下列操作,请回答有关问题:

(1)若止水夹C打开,B容器中有什么现象发生:__________________________________________。
(2)若开始时止水夹C关闭,容器A中的反应还在进行时,B容器中有什么现象发生:_________________,写出B容器中有关反应的化学方程式:_____________________。
(3)若先打开止水夹C一段时间,容器A中的反应还在进行时,再关闭止水夹C一会儿,B容器中有什么现象发生:_________________________________________________________。
【答案】 容器B中的导管口有气泡冒出 容器A中溶液进入容器B,容器B中有白色沉淀生成,沉淀迅速变为灰绿色,最后变成红褐色 2NaOH+FeSO4===Fe(OH)2↓+Na2SO4、4Fe(OH)2+O2+2H2O===4Fe(OH)3 开始时容器B中的导管口有气泡冒出,止水夹关闭后容器A中溶液进入容器B,有白色沉淀生成
【解析】
若弹簧止水夹C打开,则产生的H2经C进入B容器中产生气泡,排出空气。若关闭止水夹C,则反应产生的H2会将A中溶液压入B中而发生反应,若B中无氧气,则发生反应FeSO4+2NaOH=Fe(OH)2↓+Na2SO4;若B中有氧气,则继续发生反应4Fe(OH)2+O2+2H2O=4Fe(OH)3。
(1). 若弹簧止水夹C打开,则产生的H2经C进入B容器中产生气泡,排出空气,所以B中的现象是导管口有气泡冒出;
(2) 若开始时止水夹C关闭,仪器中混有部分空气,反应产生的H2会将A中溶液压入B中而发生反应,方程式为:FeSO4+2NaOH=Fe(OH)2↓+Na2SO4 ,Fe(OH)2为白色沉淀,遇空气中的氧气沉淀迅速变为灰绿色,最后变成红褐色的Fe(OH)3。
(3) 若先打开止水夹C一段时间,容器A中的反应还在进行,排出装置中的空气。若关闭止水夹C,则反应产生的H2会将A中溶液压入B中而发生反应,则发生反应FeSO4+2NaOH=Fe(OH)2↓+Na2SO4。

 名校课堂系列答案
名校课堂系列答案【题目】(1)Br位于元素周期表第_____周期第_____族;基态Na+核外有_____种运动状态不同的电子;Mg基态原子核外电子排布式为_____。
(2)用“>”或“<”填空:
第一电离能 | 粒子半径 | 熔点 | 键的极性 |
N_____S | S2—_____ Mg2+ | SO3______Na2O2 | H﹣O_____H﹣N |
(3)已知多硫化钠﹣溴储能电池是一种二次电池,结构如图。电池总反应为:2Na2S3+2NaBr![]() 3Na2S2+Br2。
3Na2S2+Br2。
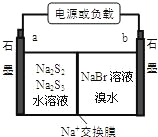
①放电时Na+向_____极迁移(填“a 或 b”);
②充电时阴极电极反应式为:______________。
(4)已知N4为正四面体结构,N﹣N键能为167kJ/mol,N≡N 键能为 942kJ/mol。写 出N4(g)转化为N2(g)的热化学方程式________________。