题目内容
13.最近推出了一种廉价环保的新能源-甲醚,它完全燃烧时发生如下反应:X+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O,则 X(甲醚)的化学式是( )| A. | C3H6O2 | B. | C2H6O | C. | C2H4O | D. | CH4O |
分析 由质量守恒定律可知,在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变.据此答题.
解答 解:甲醚完全燃烧时发生反应的方程式是X+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O,根据质量守恒定律可得,X(甲醚)的化学式中C的个数应为2个,H的个数应为3×2=6个,O的个数应为2×2+3-3×2=1个,故X(甲醚)的化学式为C2H6O.
故选B.
点评 本题考查了质量守恒定律,题目难度不大,注意在化学反应前后原子的种类、质量、个数不变,侧重于基础知识的考查.

练习册系列答案
相关题目
1.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,1.8g水中所含有氧原子数目为0.1NA | |
| B. | 常温常压下,2.24LCO2气体中含氧原子数目为0.2NA | |
| C. | 0.1mol/LCuCl2溶液中,含有Cl-离子的数目为0.2NA | |
| D. | 常温常压下,23gNa+中含有的电子数为NA |
8.由铜、锌、CuSO4溶液,ZnSO4溶液组成如图所示的原电池,则下列说法正确是( )


| A. | a极为铜,b极为锌 | |
| B. | 当正极质量增加64g时,负极质量减小65g | |
| C. | A池中盛放的是CuSO4溶液,B池中盛放的是ZnSO4溶液 | |
| D. | 盐桥中的阳离子向锌极移动,阴离子向铜极移动 |
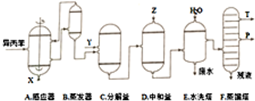
18.丙酮和苯酚都是重要的化工原料,工业上可用异丙苯氧化法生产苯酚和丙酮,其反应和工艺流程示意图如下:
① +O2$\stackrel{催化剂}{→}$
+O2$\stackrel{催化剂}{→}$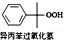 △H=-116kJ.mol-1
△H=-116kJ.mol-1
②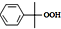 $\stackrel{H+}{→}$
$\stackrel{H+}{→}$ △H=-253kJ.mol-1
△H=-253kJ.mol-1
相关化合物的物理常数
回答下列问题:
(1)反应①和②分别在装置A和C中进行(填装置符号).
(2)反应②为放热(填“放热”或“吸热”)反应.反应温度控制在50-60℃,温度过高的安全隐患是温度过高会导致爆炸.
(3)在反应器A中通入的X是氧气或空气.
(4)在分解釜C中加入的Y为少量浓硫酸,其作用是催化剂,优点是用量少,缺点是腐蚀设备.
(5)中和釜D中加入的Z最适宜的是c(填编号.已知苯酚是一种弱酸)
a.NaOHb.CaCO3c.NaHCO3d.CaO
(6)蒸馏塔F中的馏出物T和P分别为丙酮和苯酚,判断的依据是丙酮的沸点低于苯酚.
(7)用该方法合成苯酚和丙酮的优点是原子利用率高.

①
 +O2$\stackrel{催化剂}{→}$
+O2$\stackrel{催化剂}{→}$ △H=-116kJ.mol-1
△H=-116kJ.mol-1②
 $\stackrel{H+}{→}$
$\stackrel{H+}{→}$ △H=-253kJ.mol-1
△H=-253kJ.mol-1相关化合物的物理常数
| 物质 | 相对分子质量 | 密度(g/cm-3) | 沸点/℃ |
| 苯酚 | 94 | 1.0722 | 182 |
| 丙酮 | 58 | 0.7898 | 56.5 |
| 异丙苯 | 120 | 0.8640 | 153 |
(1)反应①和②分别在装置A和C中进行(填装置符号).
(2)反应②为放热(填“放热”或“吸热”)反应.反应温度控制在50-60℃,温度过高的安全隐患是温度过高会导致爆炸.
(3)在反应器A中通入的X是氧气或空气.
(4)在分解釜C中加入的Y为少量浓硫酸,其作用是催化剂,优点是用量少,缺点是腐蚀设备.
(5)中和釜D中加入的Z最适宜的是c(填编号.已知苯酚是一种弱酸)
a.NaOHb.CaCO3c.NaHCO3d.CaO
(6)蒸馏塔F中的馏出物T和P分别为丙酮和苯酚,判断的依据是丙酮的沸点低于苯酚.
(7)用该方法合成苯酚和丙酮的优点是原子利用率高.
5.nL三种气态烃混合物与足量氧气混合点燃后,恢复到原来状态(常温常压),体积共缩小2nL,这三种烃不可能的组合是( )
| A. | CH4、C2H4、C3H4以任意比混合 | |
| B. | C2H6、C4H6、C2H2以2:1:2的物质的量之比混合 | |
| C. | C3H8、C4H8、C2H2以11:14:26的质量之比混合 | |
| D. | CH4、C3H6、C2H2以a:b:b体积比混合 |
1.t℃时,在体积不变的密闭容器中发生反应:X(g)+3Y(g)?2Z(g),各组分在不同时刻的浓度如表:下列说法正确的是( )
| 物质 | X | Y | Z |
| 初始浓度/mol•L-1 | 0.1 | 0.2 | 0 |
| 2min末浓度/mol•L-1 | 0.08 | a | b |
| 平衡浓度/mol•L-1 | 0.05 | 0.05 | 0.1 |
| A. | 平衡时,X的转化率为20% | |
| B. | t℃时,该反应的平衡常数为40 | |
| C. | 前2 min内,用Y的变化量表示的平均反应速率v(Y)=0.03 mol•L-1•min-1 | |
| D. | 增大平衡后的体系压强,v正增大,v逆减小,平衡向正反应方向移动 |
 金刚烷(C10H16)的结构如图1所示,它可以看成四个等同的六元环组成的空间构型.立方烷(C8H8)的结构如图2所示.其中金刚烷的二氯代物和立方烷的六氯代物的同分异构体数目分别是6个和3个.
金刚烷(C10H16)的结构如图1所示,它可以看成四个等同的六元环组成的空间构型.立方烷(C8H8)的结构如图2所示.其中金刚烷的二氯代物和立方烷的六氯代物的同分异构体数目分别是6个和3个.