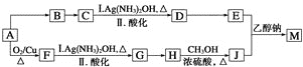
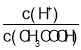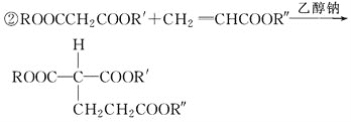题目内容
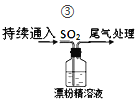
【题目】某学生对SO2与漂粉精的反应进行实验探究,下列叙述错误的是
操作 | 现象 |
①取4 g漂粉精固体,加入100 mL水 | 部分固体溶解,溶液略有颜色 |
②过滤,测漂粉精溶液的pH | pH试纸先变蓝,最后褪色 |
| 液面上方出现白雾;稍后,出现浑浊,溶液变为黄绿色;最终,产生大量白色沉淀,黄绿色褪去。 |
A.Cl2和Ca(OH)2制取漂粉精的化学方程式是:2Cl2+2Ca(OH)2 →CaCl2+Ca(ClO)2+2H2O
B.pH试纸颜色的变化说明漂粉精溶液具有碱性、漂白性
C.液面上方出现白雾,白雾中一定只含HCl
D.最后,产生大量白色沉淀,黄绿色褪去,推测白色沉淀主要是CaSO4
【答案】C
【解析】
A.Cl2和Ca(OH)2反应生成氯化钙、次氯酸钙和水,化学方程式为:2Cl2+2Ca(OH)2 →CaCl2+Ca(ClO)2+2H2O,A正确;
B.次氯酸钙为强碱弱酸盐,水解显碱性,水解生成的次氯酸具有漂白性,所以pH试纸先变蓝,最后褪色,B正确;
C.液面上方出现白雾,白雾中除了含有HCl外还含有SO2,C错误;
D.亚硫酸钙在溶液中被Cl2氧化成CaSO4,D正确;
故合理选项是C。

 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案【题目】从某含Br—废水中提取Br2的过程包括:过滤、氧化、萃取(需选择合适萃取剂)及蒸馏等步骤。已知:
物质 | Br2 | CCl4 | 正十二烷 |
密度/g·cm-3 | 3.119 | 1.595 | 0.753 |
沸点/℃ | 58.76 | 76.8 | 215~217 |
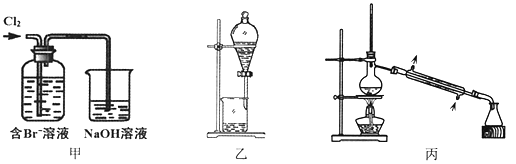
下列说法不正确的是
A. 甲装置中Br—发生的反应为:2Br-+ Cl2 = Br2 + 2Cl-
B. 甲装置中NaOH溶液每吸收0.1mol Cl2,转移0.1mol e—
C. 用乙装置进行萃取,溶解Br2的有机层在下层
D. 用丙装置进行蒸馏,先收集到的是Br2
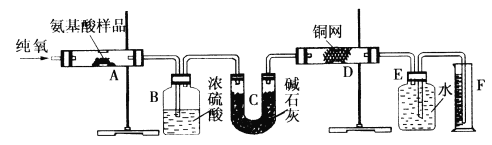
【题目】某探究小组设计如图所示装置(夹持、加热仪器略),模拟工业生产进行制备三氯乙醛(CCl3CHO)的实验。查阅资料,有关信息如下:

①制备反应原理: C2H5OH + 4Cl2→CCl3CHO+5HCl
可能发生的副反应:
C2H5OH + HCl→C2H5Cl+H2O
CCl3CHO + HClO→CCl3COOH (三氯乙酸) +HCl
②相关物质的部分物理性质:
C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
熔点/℃ | -1 14.1 | -57.5 | 58 | -138.7 |
沸点/℃ | 78.3 | 97.8 | 198 | 12.3 |
溶解性 | 与水互溶 | 可溶于水、乙醇 | 可溶于水、乙醇 | 微溶于水,可溶于乙醇 |
(1)装置B中盛放的试剂是___________;装置E的作用是_______;
(2)若撤去装置C,可能导致装置D中副产物________(填化学式)的量增加;装置D可采用________加热的方法以控制反应温度在70℃左右。
(3)反应结束后,可采用_________的方法从D中的混合物分离出CCl3COOH,除酒精灯、接液管、温度计、锥形瓶外,所需玻璃仪器有_________。
(4)测定产品纯度:称取产品0.30 g配成待测溶液,加入0.1000 mol/L碘标准溶液20.00 mL,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,立即用0.0200 mol/LNa2S2O3溶液滴定至终点。进行平行实验后,测得消耗Na2S2O3溶液20.00 mL。则产品的纯度为____。(保留3位有效数字)
滴定的反应原理:CCl3CHO +OH—→CHCl3 + HCOO- HCOO-+ I2 → H+ + 2I-+ CO2↑ I2 + 2S2O32-→2I- + S4O62-
(5)请设计实验方案证明三氯乙酸的酸性比乙酸强:________