题目内容
【题目】某小组同学设计了如下实验装置并开展研究(部分夹持装置已略去)。
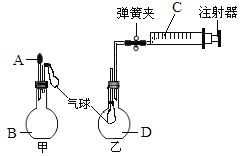
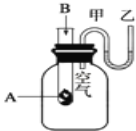
(1)当将A慢慢滴入甲瓶后,观察到甲瓶上的气球慢慢鼓起,则A和B分别可能是下列组合中的______(填选项序号)。
①稀硫酸和NaHCO3溶液 ②浓硫酸和NaOH溶液
③NaCl溶液和KNO3溶液 ④蒸馏水和NH4NO3固体
(2)将少量C慢慢推入乙瓶。
①若观察到乙瓶内的气球慢慢鼓起,且C为蒸馏水,则气体D可能为________(任填一种物质的化学式)。
②若C为O2,气体D为NO,则能观察到乙瓶中的现象是____________________。
(3)若他们利用下图所示装置进行实验。
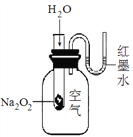
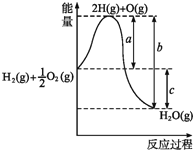
①将水滴入试管后能观察到的现象为________________,这是因为该反应为____________反应(填“放热”或“吸热”),反应物的总能量比生成物的总能量____________(填“高”或“低”,下同),反应物化学键断裂时吸收的总能量________于生成物化学键形成时放出的总能量。
②该反应的化学方程式为_______________________________,反应中能量的主要转化形式为____________________。
【答案】 ①② HCl(合理即可) 气体颜色逐渐变为红棕色,气球无明显变化 U形管内红墨水左边液面低于右边 放热 高 低 2Na2O2+2H2O=4NaOH+O2↑ 化学能转化为热能
【解析】(1)当将A慢慢滴入甲瓶后,观察到甲瓶上的气球慢慢鼓起,说明反应放热或产生气体,则①稀硫酸和NaHCO3溶液反应产生二氧化碳,正确;②浓硫酸和NaOH溶液混合反应放出热量,正确;③NaCl溶液和KNO3溶液不反应,温度变化很小,错误;④蒸馏水和NH4NO3固体混合吸热,温度降低,错误,答案选①②;(2)①若观察到乙瓶内的气球慢慢鼓起,说明瓶中压强降低,如果C为蒸馏水,则气体D易溶于水,可能为HCl、NH3等。②若C为O2,气体D为NO,二者混合反应生成二氧化氮,气体体积不变,则能观察到乙瓶中的现象是气体颜色逐渐变为红棕色,气球无明显变化。(3)①将水滴入试管后与过氧化钠反应生成氢氧化钠和氧气,反应放热,压强增大,因此能观察到的现象为U形管内红墨水左边液面低于右边,放热反应中反应物的总能量比生成物的总能量高,反应物化学键断裂时吸收的总能量低于生成物化学键形成时放出的总能量。②该反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑,反应中能量的主要转化形式为化学能转化为热能。

【题目】按照物质的树状分类和交叉分类,HNO3应属于
①酸 ②氢化物 ③氧化物 ④含氧酸 ⑤难挥发性酸⑥强酸 ⑦一元酸 ⑧化合物 ⑨混合物
A. ①②③④⑤⑥⑦⑧B. ①④⑥⑦⑧
C. ①⑨D. ①④⑤⑥⑦
【题目】某小组同学欲通过实验验证氯元素的非金属性强于硫元素。请帮他们完成实验报告。
(1)他们将过量硫粉与少量铁粉混合后隔绝空气加热,制得并分离出固体产物A。
实验步骤和操作 | 实验现象 | 实验结论或解释 |
①取少量A于试管中,加入足量稀硫酸 | 固体完全溶解,产生有臭鸡蛋气味的气体B | 硫粉与铁粉混合后隔绝空气加热,制得固体产物A是______(填化学式) |
②将B通入足量水中 | 得到无色溶液C | |
③向①的试管中加入KSCN溶液 | 溶液无明显变化 | |
④将浓盐酸滴到KMnO4固体上 | 产生黄绿色气体 | 反应生成氯气 |
⑤将红热的铁丝(少量)伸入上述黄绿色气体中 | 铁丝剧烈燃烧,产生大量棕黄色的烟 | 反应的化学方程式为 _________________ |
⑥将⑤中所得固体产物溶于水,在所得溶液中滴加KSCN溶液 | 观察到______________(填现象) |
(2)综合上述实验现象和结论,______(填“能”或“不能”)验证氯元素的非金属性强于硫元素,理由是__________________________________________________。
(3)某同学将上述实验中④所得氯气直接通入无色溶液C中,观察到产生淡黄色固体,反应的化学方程式为_______________________________,此实验______(填“能”或“不能”)验证氯元素的非金属性强于硫元素。
(4)某同学认为将步骤①中的稀硫酸换成稀盐酸,若同样产生有臭鸡蛋气味的气体B,则可以说明氯元素的非金属性强于硫元素,他的观点________(填“正确”或“错误”),原因是_________________________________________________________。