题目内容
【题目】下列有关2个电化学装置的叙述正确的是( ) 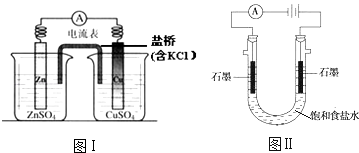
A.图Ⅰ,电流形成的完整过程是:负极Zn﹣2e﹣═Zn2+ , 电子经导线流向正极,正极Cu2++2e﹣═Cu
B.图Ⅰ,在不改变总反应的前提下,可用Na2SO4替换ZnSO4 , 用石墨替换Cu棒
C.图Ⅱ,通电后H+和Na+先从阳极区移动到阴极,然后阴极才发生反应2H++2e﹣═H2↑
D.图Ⅱ,通电后,由于OH﹣向阳极迁移,导致阳极附近pH升高
【答案】B
【解析】解:A、活泼金属锌失去电子,电极反应式为:Zn﹣2e﹣═Zn2+ , 电子沿导线流向正极,正极Cu2++2e﹣═Cu,内电路离子的定向移动,构成闭合回路,才是电流形成的完整过程,故A错误;
B、Na2SO4替换ZnSO4 , 负极仍是锌放电,原电池中的铜本身未参与电极反应,所以可用能导电的石墨替换Cu棒,故B正确;
C、溶液中氢离子来源于水的电离,氢离子浓度很小,所以通电后Na+先从阳极区移动到阴极,阴极周围的水电离出氢离子在阴放电,故C错误;
D、阳极是氯离子放电,生成酸性气体氯气,氯离子放电结束后是水电离出的氢氧根离子放电,导致阳极附近pH降低,故D错误;
故选B.

练习册系列答案
 期末集结号系列答案
期末集结号系列答案
相关题目