题目内容
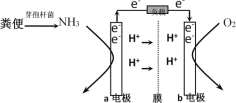
【题目】碳酸氢钠是一种重要的化工原料,在日常生活中也有广泛的用途,侯德榜先生发明了连续生产纯碱与氯化铵的联合制碱工艺,成为近代化学工业的奠基人之一,该反应原理为:![]() 饱和
饱和![]() .
.
现用如图所示装置和上述原理制取碳酸氢钠晶体,图中夹持装置已略去.
可选用的药品有:①石灰石②生石灰③![]() 盐酸④稀硫酸⑤浓氨水⑥饱和氯化钠溶液⑦饱和碳酸氢钠溶液
盐酸④稀硫酸⑤浓氨水⑥饱和氯化钠溶液⑦饱和碳酸氢钠溶液

请回答下列问题
(1)仪器a的名称是______.
(2)![]() 中应选用的药品是______
中应选用的药品是______![]() 填序号
填序号![]()
(3)在实验过程中,应先向C中通入的气体的化学式是______,其原因是______.
(4)![]() 中脱脂棉应浸润的试剂是______
中脱脂棉应浸润的试剂是______![]() 填写字母编号
填写字母编号![]()
![]() 浓硫酸
浓硫酸 ![]() 稀硫酸
稀硫酸 ![]() 氢氧化钠溶液
氢氧化钠溶液 ![]() 浓硝酸
浓硝酸
(5)该小组同学为了测定C中所得晶体中碳酸氢钠的纯度![]() 假设晶体中不含碳酸盐杂质
假设晶体中不含碳酸盐杂质![]() ,先将晶体充分干燥后,称量质量为wg,称量质量为wg,然后进行如下图所示实验:
,先将晶体充分干燥后,称量质量为wg,称量质量为wg,然后进行如下图所示实验:

![]() 操作Ⅲ中的方法是______,______,______
操作Ⅲ中的方法是______,______,______
![]() 所得晶体中碳酸氢钠的纯度是______
所得晶体中碳酸氢钠的纯度是______![]() 不必化简
不必化简![]()
【答案】圆底烧瓶 ⑦ ![]()
![]() 在水中溶解度小,先通
在水中溶解度小,先通![]() 至饱和,有利于
至饱和,有利于![]() 析出 b 过滤 洗涤 干燥
析出 b 过滤 洗涤 干燥 ![]()
【解析】
![]() 根据常用的仪器名称解答;
根据常用的仪器名称解答;
![]() 装置的作用为除去二氧化碳中的氯化氢,二氧化碳在饱和碳酸氢钠溶液中溶解度不大,氯化氢能够与碳酸氢钠反应生成二氧化碳;
装置的作用为除去二氧化碳中的氯化氢,二氧化碳在饱和碳酸氢钠溶液中溶解度不大,氯化氢能够与碳酸氢钠反应生成二氧化碳;
![]() 根据二氧化碳和氨气的溶解性判断先通入的气体,氨气极易溶于水,易于二氧化碳的吸收,所以应先通入氨气;
根据二氧化碳和氨气的溶解性判断先通入的气体,氨气极易溶于水,易于二氧化碳的吸收,所以应先通入氨气;
![]() 氨气易挥发,氨气为碱性气体,与酸反应、与碱不反应,浓硫酸具有强氧化性,浓硝酸易挥发;
氨气易挥发,氨气为碱性气体,与酸反应、与碱不反应,浓硫酸具有强氧化性,浓硝酸易挥发;
![]() 测定C中所得晶体的碳酸氢钠的纯度
测定C中所得晶体的碳酸氢钠的纯度![]() 假设晶体中不含碳酸盐杂质
假设晶体中不含碳酸盐杂质![]() ,将晶体充分干燥后,称量质量为wg,此时为碳酸氢钠粗品质量,操作1将晶体加热到质量不再变化时,所得粉末为碳酸钠和杂质,然后溶解,加入氢氧化钡溶液,氢氧化钡跟碳酸钠反应生成碳酸钡,将生成的碳酸钡过滤、洗涤、干燥,称量为ng,根据关系式
,将晶体充分干燥后,称量质量为wg,此时为碳酸氢钠粗品质量,操作1将晶体加热到质量不再变化时,所得粉末为碳酸钠和杂质,然后溶解,加入氢氧化钡溶液,氢氧化钡跟碳酸钠反应生成碳酸钡,将生成的碳酸钡过滤、洗涤、干燥,称量为ng,根据关系式![]() --
--![]() 可求出纯碳酸氢钠的质量。
可求出纯碳酸氢钠的质量。
![]() 装置为制取二氧化碳的装置,仪器a为圆底烧瓶,故答案为:圆底烧瓶;
装置为制取二氧化碳的装置,仪器a为圆底烧瓶,故答案为:圆底烧瓶;
![]() 装置的作用为除去二氧化碳中的氯化氢,二氧化碳在饱和碳酸氢钠溶液中溶解度不大,氯化氢能够与碳酸氢钠反应生成二氧化碳,所以B中盛有试剂为饱和碳酸氢钠溶液,
装置的作用为除去二氧化碳中的氯化氢,二氧化碳在饱和碳酸氢钠溶液中溶解度不大,氯化氢能够与碳酸氢钠反应生成二氧化碳,所以B中盛有试剂为饱和碳酸氢钠溶液,
故答案为:![]() ;
;
![]() 在水中溶解度小,氨气极易溶于水,则先通
在水中溶解度小,氨气极易溶于水,则先通![]() 至饱和,然后通入二氧化碳气体,有利于
至饱和,然后通入二氧化碳气体,有利于![]() 析出,
析出,
故答案为:![]() ;
;![]() 在水中溶解度小,先通
在水中溶解度小,先通![]() 至饱和,有利于
至饱和,有利于![]() 析出;
析出;
![]() 氨气易挥发,D中脱脂棉应浸润的试剂吸收逸出的氨气,浓硫酸能使棉花脱水、浓硝酸具有挥发性,氨气为碱性气体,与硫酸反应,所以选择稀硫酸,
氨气易挥发,D中脱脂棉应浸润的试剂吸收逸出的氨气,浓硫酸能使棉花脱水、浓硝酸具有挥发性,氨气为碱性气体,与硫酸反应,所以选择稀硫酸,
故答案为:b;
![]() 测定C中所得晶体的碳酸氢钠的纯度
测定C中所得晶体的碳酸氢钠的纯度![]() 假设晶体中不含碳酸盐杂质
假设晶体中不含碳酸盐杂质![]() ,将晶体充分干燥后,称量质量为wg,此时为碳酸氢钠粗品质量,操作1将晶体加热到质量不再变化时,所得粉末为碳酸钠和杂质,然后溶解,加入氢氧化钡溶液,氢氧化钡跟碳酸钠反应生成碳酸钡,将生成的碳酸钡过滤、洗涤、干燥,称量为
,将晶体充分干燥后,称量质量为wg,此时为碳酸氢钠粗品质量,操作1将晶体加热到质量不再变化时,所得粉末为碳酸钠和杂质,然后溶解,加入氢氧化钡溶液,氢氧化钡跟碳酸钠反应生成碳酸钡,将生成的碳酸钡过滤、洗涤、干燥,称量为![]() ,
,
反应的化学方程式为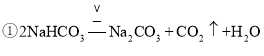 ,
,![]() ,得到的碳酸钡需要经过过滤、洗涤、干燥后方可称量.
,得到的碳酸钡需要经过过滤、洗涤、干燥后方可称量.
设样品中碳酸氢钠的质量为x,由上两式可得关系式:
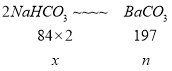
![]() ,
,![]() ,
,
所得晶体中碳酸氢钠的纯度![]() 。
。