题目内容
【题目】可逆反应NO2(g)+ CO(g) ![]() CO2(g)+ NO(g) 反应过 程中的能量变化如图所示,下列说法正确的是
CO2(g)+ NO(g) 反应过 程中的能量变化如图所示,下列说法正确的是
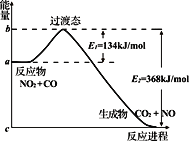
A. 1molNO2与1molCO混合经充分反应放热234 kJ
B. 若反应开始时加入催化剂, 则使E1 、E2 都变大
C. 正反应的活化能是134kJ/mol
D. 该反应的反应热⊿H = E2–E1
【答案】C
【解析】A、此反应是可逆反应,不能完全进行到底,因此1molNO2与1molCO混合充分反应放出的热量小于234kJ,故A错误;B、使用催化剂,降低活化能,E1和E2都降低,故B错误;C、根据图像,正反应的活化能是134kJ·mol-1,故C正确;D、反应物的总能量大于生成物的总能量,此反应是放热反应,△H<0,因此△H=E1-E2,故D错误。

练习册系列答案
相关题目
【题目】物质的分离与提纯是化学实验研究常用的方法。下列混合体系分离提纯对应的方法不正确的是( )
选项 | A | B | C | D |
混合 体系 | 溴水 | 酒精与水 | 固体碘和氯化铵 | 混有少量KCl的KNO3粉末 |
分离 方法 | 萃取、分液 | 加生石灰,蒸馏 | 加热 | 配成热的饱和溶液,降温结晶 |
A. A B. B C. C D. D