题目内容
【题目】工业上利用电镀污泥(主要含有Fe2O3、CuO、Cr2O3及部分难溶杂质)回收铜和铬等金属,回收流程如下:
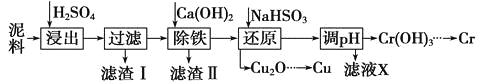
已知部分物质沉淀的pH及CaSO4的溶解度曲线如下:
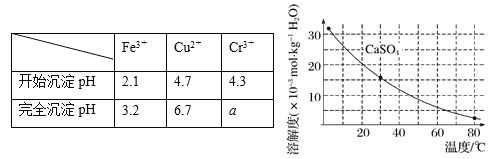
(1)在浸出过程中除了生成Fe2(SO4)3、Cr2(SO4)3外,主要还有 。
(2)在除铁操作中,需要除去Fe3+和CaSO4,请完成相关操作:
①加入石灰乳调节pH范围 ,检验Fe3+已经除尽的操作是 ;
②将浊液加热到80℃, 。
(3)写出还原步骤中加入NaHSO3生成Cu2O固体反应的离子方程式: ,此步骤中加入NaHSO3得到Cu2O的产率为95%,若NaHSO3过量,除了浪费试剂外,还会出现的问题是 。
(4)当离子浓度小于或等于1×10-5 mol·L-1时可认为沉淀完全,若要使Cr3+完全沉淀则要保持c(OH-)≥ 。[已知:Ksp[Cr(OH)3] = 6.3×10-31,![]() ≈4.0]。
≈4.0]。
【答案】(1)CuSO4
(2)①3.2~4.3取适量滤液,加KSCN溶液,若不变红,则说明Fe3+已除②趁热过滤
(3)2H2O+HSO3-+2Cu2+=Cu2O↓+SO42-+5H+产生SO2,污染环境
(4)4.0×10-9mol·L-1
【解析】试题分析:(1)Fe2O3、CuO、Cr2O3均能溶于硫酸,分别生成盐[Fe2(SO4)3、CuSO4、Cr2(SO4)3]和水;(2)由部分物质沉淀的pH及除铁操作的目的可知,加入石灰乳调节溶液的pH为3.2~4.3,不会沉淀Cu2+、Cr3+,但能除去Fe3+和CaSO4;Fe3+遇KSCN变红,如果溶液中Fe3+已经除尽,则滤液遇KSCN溶液不变红;再由CaSO4的溶解度曲线可知,CaSO4的溶解度随温度升高而逐渐减小,如果将浊液加热到80℃,趁热过滤,可以除去CaSO4;(3)由铜元素降价可知硫元素必须升价,根据易溶且完全电离的化合物拆写原则、电子电荷原子守恒可知,还原步骤的原理为![]() ;亚硫酸属于中强酸,而还原步骤可以生成的硫酸是强酸,若NaHSO3过量,过量的NaHSO3可以与强酸反应生成有毒的SO2气体,造成环境污染;(4)由沉淀溶解原理可知,Cr(OH)3(s)
;亚硫酸属于中强酸,而还原步骤可以生成的硫酸是强酸,若NaHSO3过量,过量的NaHSO3可以与强酸反应生成有毒的SO2气体,造成环境污染;(4)由沉淀溶解原理可知,Cr(OH)3(s)![]() Cr3++ 3OH-,Ksp[Cr(OH)3] = c(Cr3+)c3(OH-) = 6.3×10-31,则c3(OH-) = 6.3×10-31/1×10-5= 6.3×10-26= 63×10-27,c(OH-) =
Cr3++ 3OH-,Ksp[Cr(OH)3] = c(Cr3+)c3(OH-) = 6.3×10-31,则c3(OH-) = 6.3×10-31/1×10-5= 6.3×10-26= 63×10-27,c(OH-) =![]() mol·L-1= 4.0×10-9 mol·L-1,即要使Cr3+完全沉淀则要保持 c(OH-)≥4.0×10-9 mol·L-1。
mol·L-1= 4.0×10-9 mol·L-1,即要使Cr3+完全沉淀则要保持 c(OH-)≥4.0×10-9 mol·L-1。

 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案