题目内容
有某二价金属氧化物和某三价金属氧化物的等物质的量组成的混合物,两者质量比为28:51,取这种混合物19.75g,恰好能与166mL浓度为20%、密度为1.10g/cm3的盐酸反应。试求这两种金属的相对原子质量。
40、27
试题分析:设二价金属的相对原子质量为 x,三价金属相对原子质量为y。则化学式分别为:AO,B2O3.化学式量分别为:x+16,2y+48。等物质的量组成的混合物,两者质量之比为(x+16):(2y+48)=28:51,得出:51x-56y=528, AO+2HCl=ACl2+H2O, B2O3+6HCl=2BCl3+3H2O
设与两种金属氧化物反应的盐酸分别为M,N (x+16):2×36.5=28×19.75/(28+51):M,(2y+48):6×36.5=51×19.75/(28+51):N M+N=(1000×1.1×20%)×0.166/36.5="1" 计算即可。

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
 B.
B. C.
C. D.
D.

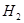 所占的体积一定是22.4L
所占的体积一定是22.4L 溶液中,含有
溶液中,含有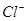 的个数为
的个数为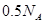
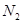 和CO的混合气体,其体积约为22.4L
和CO的混合气体,其体积约为22.4L 2CaO+O2↑+2nH2O,2CaO2+4HCl=2CaCl2+2H2O+O2↑。现称取2.168 g过氧化钙样品分成两等份进行下列实验:
2CaO+O2↑+2nH2O,2CaO2+4HCl=2CaCl2+2H2O+O2↑。现称取2.168 g过氧化钙样品分成两等份进行下列实验: