题目内容
【题目】T℃时,向![]() 恒容密闭容器中充入
恒容密闭容器中充入![]() ,发生反应
,发生反应![]() 。反应过程中
。反应过程中![]() 随时间变化的曲线如图所示,下列说法不正确的是( )
随时间变化的曲线如图所示,下列说法不正确的是( )
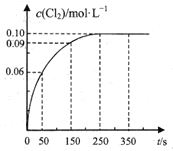
A.反应在![]() 的平均速率
的平均速率![]()
B.该温度下,反应的平衡常数值![]()
C.保持其他条件不变,升高温度,若平衡时![]() ,则该反应的
,则该反应的![]()
D.反应达平衡后,再向容器中充入![]() ,该温度下再达到平衡时,
,该温度下再达到平衡时,![]()
【答案】D
【解析】
A.由图可知,0~50s 内Cl2的浓度变化量为0.06mol/L,![]() ,A正确;
,A正确;
B.由图可知,250s时达到平衡,平衡时c(Cl2)=0.10mol/L,则:

该温度下平衡常数![]() ,B正确;
,B正确;
C.平衡时c(PCl3)=0.10mol/L,保持其他条件不变,升高温度,平衡时c′(PCl3)=0.11mol/L,浓度增大,平衡向正反应移动,该反应正反应为吸热反应,△H>0,C正确;
D.反应达平衡后,再向容器中充入 1mol PCl5,相当于增大压强,平衡向逆反应方向进行,与原平衡相比PCl5转化率降低,达到平衡时0.1mol/L<c(Cl2)<0.2mol/L,D错误;
故答案为:D。

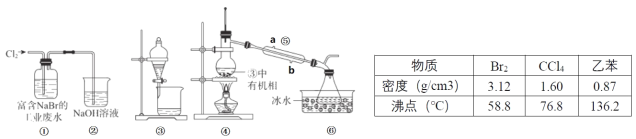
【题目】学习小组探究AgNO3、Ag2O(棕黑色固体,难溶于水)对氯水漂白性的影响。
实验记录如下:
| 实验 | 方案和现象 |
ⅰ | 加入1mL蒸馏水,再滴加1滴品红溶液,品红溶液较快褪色 | |
ⅱ | 加入少量Ag2O固体,产生白色沉淀a。再加入1mL蒸馏水和 1滴品红溶液,品红溶液褪色比i快 | |
ⅲ | 加入1mL较浓AgNO3溶液,产生白色沉淀b。再滴加1滴品红溶液,品红溶液褪色比i慢 |
(1)用离子方程式表示i中品红溶液褪色的原因:______。
(2)经检验,ii中的白色沉淀a是AgCl。产生AgCl的化学方程式是_______。
(3)ⅰ是iii的对比实验,目的是排除iii中______造成的影响。
(4)研究白色沉淀b的成分。进行实验iv(按实验iii的方案再次得到白色沉淀b,过滤、洗涤,置于试管中):
实验iv:
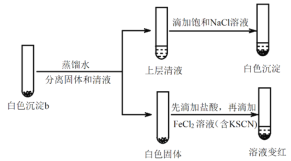
①设计对比实验证实白色沉淀b不只含有AgCl,实验方案和现象是_______。
②FeCl2溶液的作用是_______。由此判断,白色沉淀b可能含有AgClO。
(5)进一步研究白色沉淀b和实验iii品红溶液褪色慢的原因,进行实验v:
实验v:

①结合离子方程式解释加入饱和NaCl溶液的目的:_______。
②推测品红溶液褪色的速率:实验iii比实验v______(填“快”或 “慢”)。