题目内容
【题目】一学生用如图装置研究原电池原理,下列说法错误的是( )
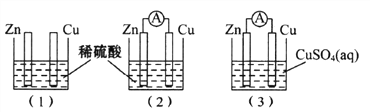
A. (1)图中铜棒上没有气体产生
B. (2)图中如果两极上都有气体产生,则说明锌片不纯
C. (2)图与(3)图中正极生成物质质量比为1:32时,锌片减轻的质量相等
D. (3)图中锌片增重质量与铜棒减轻质量的比值为65:64
【答案】D
【解析】A、装置图1是化学腐蚀,锌和稀硫酸发生反应生成氢气,铜和稀硫酸不反应,图1中铜棒上没有气体产生,故A正确;B、图2是原电池装置,锌做负极,铜做正极溶液中氢离子在铜电极生成氢气,锌片不纯会形成原电池,锌片表面也有气体生成,故B正确;C、(2)图与(3)图中电极反应负极Zn-2e-=Zn2+,图2中正极上电极反应2H++2e-=H2↑,图3中正极电极反应为Cu2++2e-=Cu,正极生成物质质量比为1:32时,依据电子守恒计算两个原电池中电子转移相同,所以反应的锌的质量相同,故C正确;D、图3是原电池装置,锌做负极失电子生成锌离子,铜做正极,溶液中铜离子得到电子生成铜,锌电极减轻,铜电极增重,故D错误;故选D。

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
【题目】用图中所示的装置进行实验,实验现象与预测不一致的是( )
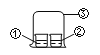
选项 | ①中的物质 | ②中的物质 | 预测现象 |
A | 浓氨水 | FeCl3溶液 | ②中有红褐色沉淀 |
B | 浓氨水 | 浓盐酸 | ③中有白烟 |
C | 浓硝酸 | 淀粉KI溶液 | ②中溶液无明显变化 |
D | 浓盐酸 | 酚酞溶液 | ②中溶液无明显变化 |
A. A B. B C. C D. D