题目内容
在2H2S+SO2=2H2O+3S中氧化剂与还原剂物质的量之比为( )
| A.2∶1 | B.3∶2 |
| C.1∶2 | D.2∶3 |
C
解析试题分析:该反应中硫化氢是还原剂,二氧化硫是氧化剂,因此氧化剂与还原剂物质的量之比为1∶2。
考点:考查氧化还原反应。

练习册系列答案
相关题目
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2 g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示。下列分析或结果错误的是( )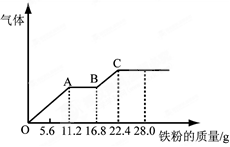
| A.H2SO4浓度为2.5 mol·L-1 |
| B.OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气 |
| C.第二份溶液中最终溶质为FeSO4 |
| D.混合酸中NO3-物质的量为0.4mol |
化学工业是国民经济的支柱产业,下列生产过程中不涉及氧化还原反应的是
| A.氮肥厂用氮气和氢气合成氨气 | B.硝酸厂用氨氧化法制硝酸 |
| C.从海水中提溴 | D.纯碱厂用NaCl、NH3、CO2等制纯碱 |
一定量的CuS和Cu2S的混合物投入足量的HNO3中,收集到气体VL(标准状况),向反应后的溶液中(存在Cu2+和SO42-)加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到CuO 12.0 g,若上述气体为NO和NO2的混合物,且体积比为1﹕1,则V可能为
| A.135 L | B.90 L | C.168 L | D.157 L |
下列物质久置于空气中会发生相应的变化,其中发生了氧化还原反应的是( )
| A.浓硫酸的质量增加 | B.铝的表面生成致密的氧化物薄膜 |
| C.澄清的石灰水变浑浊 | D.氢氧化钠固体发生潮解 |
下列叙述正确是的
| A.人工固氮的过程一定涉及到氧化还原反应 |
| B.1mol氯气在反应中一定得到2mol电子 |
| C.1mol钠在足量氧气中燃烧生成Na2O2,失去2mol电子 |
| D.发生化学反应时,失去电子越多的金属原子,还原能力越强 |
氢化亚铜(CuH)是一种不稳定物质,能在氯气中燃烧;也能与酸反应。用CuSO4溶液和“某物质”在40~50℃时反应可产生它。下列有关叙述中错误的是
| A.“某物质”具有还原性 |
| B.CuH与盐酸反应,可能产生H2 |
| C.CuH与足量的稀硝酸反应:CuH+ 3H++ NO3-→ Cu2++ NO↑+ 2H2O |
| D.CuH在氯气中燃烧:CuH+ Cl2→ CuCl+ HCl |
氢化亚铜(CuH)是一种不稳定物质,能在氯气中燃烧;也能与酸反应。用CuSO4溶液和“某物质”在40~50℃时反应可产生它。下列有关叙述中错误的是( )
| A.这“某物质”具有还原性 |
| B.CuH与盐酸反应,可能产生H2 |
| C.CuH与足量的稀硝酸反应:CuH+3H++NO3—=Cu2++NO↑+2H2O |
| D.CuH在氯气中燃烧:CuH+Cl2=CuCl+HCl |
下列说法正确的是( )。
| A.反应Na→Na2O→Na2O2中钠元素被连续氧化 |
| B.1 mol金属钠发生反应Na→Na2O和发生反应Na→Na2O2转移电子数相等 |
| C.1 mol Cl2与足量Fe反应转移3 mol电子 |
| D.将1 mol Cl2通入1 L水中转移的电子为1 mol |