题目内容
【题目】在2 L密闭容器内,充入一定量的NO和O2,800 ℃时发生反应2NO(g)+O2(g) ![]() 2NO2(g),n(NO)随时间的变化如表:
2NO2(g),n(NO)随时间的变化如表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)反应在1 s~2 s内,O2的物质的量减少________mol。
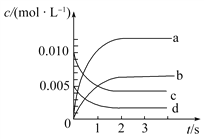
(2)如图所示,表示NO2变化曲线的是________。用O2表示从0~2s内该反应的平均速率v=________。
(3)能说明该反应已达到平衡状态的是________(填序号)。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
【答案】 0.001 b 1.5×103 mol·(L·s)1 bc
【解析】(1)根据表中信息,1 s~2 s内NO的物质的量减小0.010 mol0.008 mol=0.002 mol,NO与O2的化学计量数之比为2∶1,所以O2的物质的量减小0.001 mol。(2)由平衡体系2NO(g)+O2(g) ![]() 2NO2(g)知NO2为生成物,n(NO2)=Δn(NO)=0.020 mol0.007 mol=0.013 mol,c(NO2)=
2NO2(g)知NO2为生成物,n(NO2)=Δn(NO)=0.020 mol0.007 mol=0.013 mol,c(NO2)= ![]() =0.006 5 mol·L1,故表示NO2变化曲线的为b。v(NO)=
=0.006 5 mol·L1,故表示NO2变化曲线的为b。v(NO)= ![]() =
=![]() =0.003 mol·(L·s)1,则v(O2)=
=0.003 mol·(L·s)1,则v(O2)= ![]() v(NO)=0.001 5 mol·(L·s)1。(3)a、未指明正、逆反应速率,故无法说明该反应是否达到平衡状态,a错误;b、由于该反应是反应前后气体体积不相等的反应,当容器内压强保持不变时,说明该反应已达到平衡状态,b正确;c、已说明正、逆反应速率相等,故说明该反应已达到平衡状态,c正确;d、由于气体总质量不变,容器总体积也不变,因此,无论该反应是否达到平衡,容器内密度总保持不变,不能说明该反应达到平衡状态,d错误,答案选bc。
v(NO)=0.001 5 mol·(L·s)1。(3)a、未指明正、逆反应速率,故无法说明该反应是否达到平衡状态,a错误;b、由于该反应是反应前后气体体积不相等的反应,当容器内压强保持不变时,说明该反应已达到平衡状态,b正确;c、已说明正、逆反应速率相等,故说明该反应已达到平衡状态,c正确;d、由于气体总质量不变,容器总体积也不变,因此,无论该反应是否达到平衡,容器内密度总保持不变,不能说明该反应达到平衡状态,d错误,答案选bc。

 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案【题目】CoO是电子陶瓷所需的重要原料,工业上可用含有Co2O3、Fe2O3、Li和Al等物质的废料制备CoO。生产流程如下:
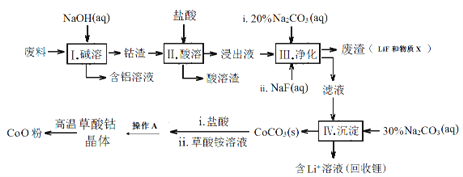
已知:① Li2CO3微溶于水;
②部分金属离子形成氢氧化物沉淀的pH见下表:
Fe3+ | Co2+ | Co3+ | Al3+ | |
pH(开始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
(1)步骤Ⅱ中酸溶时发生了反应:Co2O3+6H++2Cl-=2 + ↑+ 3H2O,_______此反应的目的是_____________。
(2)步骤Ⅲ中加入Na2CO3溶液的作用是___________,物质X的化学式为___________。
(3)步骤Ⅲ中加入NaF对步骤Ⅳ所起的作用是___________。
(4)将所得的草酸钴14.7g高温灼烧,其热重分析图如右图:
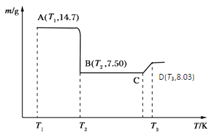
写出B点物质的化学式:___________,CD段发生反应的化学方程式为:_________________________。