题目内容
在固定体积的密闭容器中进行如下反应:2SO2(g) + O2(g)  2 SO3(g)。已知反应过程某一时刻SO2、O2、SO3浓度(mol?L-1)分别为0.2、0.1、0.2,达到平衡时,浓度可能正确的是( )
2 SO3(g)。已知反应过程某一时刻SO2、O2、SO3浓度(mol?L-1)分别为0.2、0.1、0.2,达到平衡时,浓度可能正确的是( )
| A.SO2、O2分别为0.4mol?L-1、0.2mol?L-1 | B.SO2为0.25mol?L-1 |
| C.SO2、SO3均为0.15mol?L-1 | D.SO3为0.4mol?L-1 |
B
解析试题分析:用假设法、三行数据法先求逆反应进行到底时各组分浓度的极限值,再求正反应进行到底时各组分浓度的极限值,然后根据可逆反应不能进行到底或转化率不可能是100%判断各组分浓度的取值范围,从而确定答案。先假设逆反应进行到底,则:
2SO2(g) + O2(g)  2 SO3(g)
2 SO3(g)
各组分的起始浓度/ mol?L-1 0.2 0.1 0.2
各组分的变化浓度/ mol?L-1 0.2 0.1 0.2
各组分的平衡浓度/ mol?L-1 0.4 0.2 0
再假设正反应进行到底,则:
2SO2(g) + O2(g)  2 SO3(g)
2 SO3(g)
各组分的起始浓度/ mol?L-1 0.2 0.1 0.2
各组分的变化浓度/ mol?L-1 0.2 0.1 0.2
各组分的平衡浓度/ mol?L-1 0 0 0.4
由于正、逆反应都不可能进行到底,则达到平衡时二氧化硫的浓度:0<c(SO2)<0.4 mol?L-1,氧气的浓度:0<c(O2)<0.2 mol?L-1,三氧化硫的浓度:0<c(SO3)<0.4 mol?L-1,故AD均错,B正确;若二氧化硫的浓度减小,说明反应正向进行,则三氧化硫的浓度增大,不可能二者同时减小,故C错。
考点:考查可逆反应的特点,涉及物质的量在化学方程式中的应用、可逆反应、各组分三行数据(起始浓度、变化浓度、平衡浓度)的关系、各组分浓度的极限值和取值范围、反应物浓度和生成物浓度变化关系等。

 阅读快车系列答案
阅读快车系列答案下列事实不能用勒夏特列原理解释的是
| A.配制氯化铁溶液时,加入少量稀盐酸 |
| B.配制氯化亚铁溶液时,加入少量铁屑 |
| C.在含有酚酞的氨水中加入少量NH4Cl,溶液颜色会变浅 |
| D.在硫酸铜饱和溶液中加入一块胆矾,晶体外形变规则 |
如图所示,隔板I固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:A(g) + 2B(g) xC(g)ΔH=-192kJ·mol-1,向M、N中都通入1molA和2molB的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是 ( )
xC(g)ΔH=-192kJ·mol-1,向M、N中都通入1molA和2molB的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是 ( )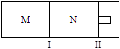
| A.若x=3,达到平衡后A的体积分数关系为:φ(M)>φ(N) |
| B.若x>3,达到平衡后B的转化率关系为:α(M)>α(N) |
| C.若x<3,C的平衡浓度关系为:c(M)>c(N) |
| D.x不论为何值,起始时向N容器中充入任意值的C,平衡后N容器中A的浓度均相等 |
PCl3和PCl5都是重要的化工原料。将PCl3(g)和Cl2(g)充入体积不变的2 L密闭容器中,在一定条件下发生反应,在10 min时达到平衡:PCl3(g)+Cl2(g) PCl5(g)。有关数据如下:
PCl5(g)。有关数据如下:
| | PCl3(g) | Cl2(g) | PCl5(g) |
| 初始浓度/(mol/L) | 2.0 | 1.0 | 0 |
| 平衡浓度/(mol/L) | c1 | c2 | 0.4 |
下列判断错误的是
A.10 min内,v(Cl2)=0.04 mol/(L·min)
B.当反应达到平衡时,容器中Cl2为1.2 mol
C.若升高温度反应的平衡常数减小,则平衡时PCl3的转化率变大
D.平衡后再加入2.0 mol PCl3,在相同条件下再达平衡时,c(PCl5)<1.0mol/L
在一密闭容器中发生反应:2X(g)+Y(g) aZ(g) △H=QkJ·mol-1,开始按体积比2:1将X、Y充入反应器中,一定条件下发生反应。图甲和图乙是根据反应绘制的图像,下列有关说法正确的是
aZ(g) △H=QkJ·mol-1,开始按体积比2:1将X、Y充入反应器中,一定条件下发生反应。图甲和图乙是根据反应绘制的图像,下列有关说法正确的是
| A.图甲,P1>P2,a < 3 |
| B.图甲,T1<T2,Q>0 |
| C.图乙,t1时表示恒温、恒压条件下,向平衡体系中充入一定量的Z气体 |
| D.图乙,如果a=3, t2时表示向体系中加入了催化剂 |
一定条件下,化学反应方向的判据为:△G=△H-T△S。已知反应A(s)= D(g)+E(g),△H-T△S=(-4499+11T)J/mol,(温度单位为K)。要防止A分解反应发生,温度必须( )
| A.高于或等于409K | B.低于136K |
| C.高于136K而且低于409K | D.任意温度 |

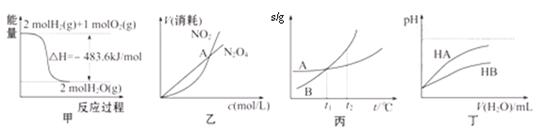
 N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动 2C(g) ΔH<0。2min后,反应达到平衡,生成C为1.6mol。则下列分析正确的是 ( )
2C(g) ΔH<0。2min后,反应达到平衡,生成C为1.6mol。则下列分析正确的是 ( )