题目内容
(7分)经研究知Cu2+对H2O2分解也具有催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某研究小组的同学分别设计了如图甲、乙所示的实验。回答相关问题:
(1) 定性分析:如图甲可通过观察________________________________,定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是__________________________________,写出H2O2在MnO2作用下发生反应的化学方程式:______________________________。
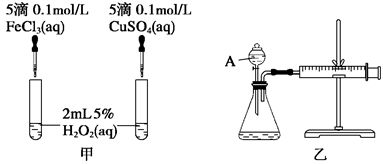
(2) 定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为__________,实验中需要测量的数据是_ _______________。
(1) 定性分析:如图甲可通过观察________________________________,定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是__________________________________,写出H2O2在MnO2作用下发生反应的化学方程式:______________________________。

(2) 定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为__________,实验中需要测量的数据是_ _______________。
(1) 反应产生气泡的快慢 (1分) 控制阴离子相同,排除阴离子的干扰 (1分)
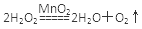 (2分)
(2分)
(2) 分液漏斗(1分) 收集40 mL气体所需要的时间(2分)
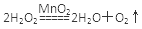 (2分)
(2分)(2) 分液漏斗(1分) 收集40 mL气体所需要的时间(2分)
首先明确实验目的:比较Fe3+和Cu2+对H2O2分解的催化效果;
(1)图甲:两试管中盛有等体积、等浓度的H2O2,分别滴入氯化铁、硫酸铜溶液,通过产生气泡的快慢即可比较Fe3+和Cu2+对H2O2分解的催化效果(保持其他条件相同,只改变催化剂);
氯离子中氯为-1价,有还原性,H2O2有氧化性,故Cl-和H2O2可发生氧化还原反应,应排除Cl-的干扰;
(2)“收集40 mL气体所需要的时间”即通过计算分别用Fe3+、Cu2+催化时生成O2的速率,来定量比较Fe3+和Cu2+对H2O2分解的催化效果;
(1)图甲:两试管中盛有等体积、等浓度的H2O2,分别滴入氯化铁、硫酸铜溶液,通过产生气泡的快慢即可比较Fe3+和Cu2+对H2O2分解的催化效果(保持其他条件相同,只改变催化剂);
氯离子中氯为-1价,有还原性,H2O2有氧化性,故Cl-和H2O2可发生氧化还原反应,应排除Cl-的干扰;
(2)“收集40 mL气体所需要的时间”即通过计算分别用Fe3+、Cu2+催化时生成O2的速率,来定量比较Fe3+和Cu2+对H2O2分解的催化效果;

练习册系列答案
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案
相关题目
 2C(g)若经2s 后测得C的浓度为0.6mol?L-1现有下列几种说法,
2C(g)若经2s 后测得C的浓度为0.6mol?L-1现有下列几种说法, 2C(气)若经 2 秒后测得 C 的浓度为0.6 mol·L-1 ,现有下列几种说法:①用物质 A 表示反应的平均速率为 0.3 mol·L-1·s-1②用物质 B 表示的反应的平均速率为 0.6 mol·L-1·s-1③ 2 s 时物质 A 的转化率为30% ④ 2 s 时物质 B 的浓度为 1.4 mol·L-1 ,其中正确的是
2C(气)若经 2 秒后测得 C 的浓度为0.6 mol·L-1 ,现有下列几种说法:①用物质 A 表示反应的平均速率为 0.3 mol·L-1·s-1②用物质 B 表示的反应的平均速率为 0.6 mol·L-1·s-1③ 2 s 时物质 A 的转化率为30% ④ 2 s 时物质 B 的浓度为 1.4 mol·L-1 ,其中正确的是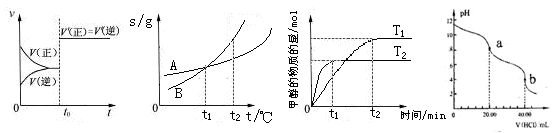 图4 图5 图6 图7
图4 图5 图6 图7 2SO3(g);已知反应过程中某一时刻,SO2、O2、SO3分别是0.2mol/L、0.1mol/L、0.2mol/L,当反应达到平衡时,可能存在的数据是
2SO3(g);已知反应过程中某一时刻,SO2、O2、SO3分别是0.2mol/L、0.1mol/L、0.2mol/L,当反应达到平衡时,可能存在的数据是 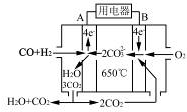
 pC(g) △H<0,平衡时测得A的浓度为0.5mol/L保持温度不变,将容器的容积缩小到原来的一半,再达平衡时测得A的浓度为1.2mol/L下列有关判断正确的是
pC(g) △H<0,平衡时测得A的浓度为0.5mol/L保持温度不变,将容器的容积缩小到原来的一半,再达平衡时测得A的浓度为1.2mol/L下列有关判断正确的是