题目内容
有关①100ml 0.1 mol/L 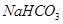 、②100ml 0.1 mol/L
、②100ml 0.1 mol/L 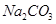 两溶液叙述不正确的是
两溶液叙述不正确的是
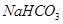 、②100ml 0.1 mol/L
、②100ml 0.1 mol/L 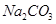 两溶液叙述不正确的是
两溶液叙述不正确的是A.溶液中水电离出的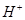 个数:②>① 个数:②>① | B.溶液中阴离子的物质的量浓度之和:②>① |
C.①溶液中: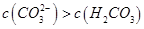 | D.②溶液中: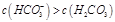 |
C
选项A:因HCO3-的水解程度大于其电离程度,所以NaHCO3溶液显碱性;由于CO32-水解使得
Na2CO3溶液也显碱性。根据越弱越水解原理可知,HCO3-的水解程度小于CO32-,弱离
子水解程度越大,对水的电离程度,所以相同浓度的NaHCO3和Na2CO3溶液中,水电
离出的H+个数:②>①,所以A正确
选项B:HCO3-水解生成H2CO3和OH-,即消耗一个HCO3-的同时又生成一个OH-,水解的过程
中阴离子数不变;
但CO32-的第一级水解生成HCO3-和OH-,即消耗一个CO32-的同时却生成了两个阴离
子,水解的过程中,阴离子总数在增加;由于起始时CO32-和HCO3-的浓度相同,所以
溶液中阴离子的物质的量浓度之和:②>①,所以B正确
选项C:因HCO3-的水解程度大于其电离程度,所以①溶液中:c(H2CO3)>c(CO32-)
所以C错
选项D:CO32-的第一级水解生成HCO3-,第二级水解生成H2CO3,且以第一级水解为主,所以②
溶液中:c(HCO3-)>c(H2CO3),所以D正确

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
 mol/L的Na2CO3、FeCl3溶液,在Na2CO3溶液中滴入酚酞,则溶液呈现________(填“浅红”或“红色”,原因:__________________________(用离子方程表达),加热,则颜色变_________(浅或深),在FeCl3溶液中滴入石蕊,,则溶液呈现________(填颜色),若将其蒸干并灼烧,则得到的固体物质为:__________________________,若将饱和的FeCl3滴入沸水,则发生的反应: _________________________(用离子方程表达)
mol/L的Na2CO3、FeCl3溶液,在Na2CO3溶液中滴入酚酞,则溶液呈现________(填“浅红”或“红色”,原因:__________________________(用离子方程表达),加热,则颜色变_________(浅或深),在FeCl3溶液中滴入石蕊,,则溶液呈现________(填颜色),若将其蒸干并灼烧,则得到的固体物质为:__________________________,若将饱和的FeCl3滴入沸水,则发生的反应: _________________________(用离子方程表达)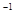 NH4Cl和0.1 mol·L
NH4Cl和0.1 mol·L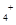 )>c(Cl
)>c(Cl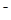 )>c(Na
)>c(Na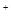 )>c(OH
)>c(OH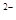 )+c(HS
)+c(HS 生成剧毒的HCN。完成下列问题:
生成剧毒的HCN。完成下列问题: 0.2mol。②_ __和_ __两种粒子的物质的量
0.2mol。②_ __和_ __两种粒子的物质的量