题目内容
镍镉(Ni—Cd)可充电电池在现代生活中有广泛应用,它的充放电反应按下式进行:
Cd(OH)2+2Ni(OH)2 Cd+2NiO(OH)+2H2O 由此可知,该电池放电时的负极材料是 ( )
Cd+2NiO(OH)+2H2O 由此可知,该电池放电时的负极材料是 ( )
| A.Cd(OH)2 | B.Ni(OH)2 | C.Cd | D.NiO(OH) |
C
解析试题分析:根据镍镉可充电电池在放电时的反应原理可知:Cd发生氧化反应,失去电子,因此作该电池的负极材料。因此选项为C。
考点:考查电极反应与电极材料的关系的知识。

 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案下列反应能设计成原电池提供电能的是
| A.Cu与Cl2燃烧反应 | B.Ba(OH)2·8H2O与NH4Cl反应 |
| C.灼热的炭与CO2反应 | D.氢氧化钠溶液与稀盐酸反应 |
硫-钠原电池具有输出功率较高,循环寿命长等优点。其工作原理可表示为:2Na+xS Na2Sx。但工作温度过高是这种高性能电池的缺陷,科学家研究发现,采用多硫化合物(
Na2Sx。但工作温度过高是这种高性能电池的缺陷,科学家研究发现,采用多硫化合物(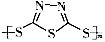 )作为电极反应材料,可有效地降低电池的工作温度,且原材料价廉、低毒,具有生物降解性。下列有关叙述正确的是
)作为电极反应材料,可有效地降低电池的工作温度,且原材料价廉、低毒,具有生物降解性。下列有关叙述正确的是
A.多硫化合物( )是一种新型无机非金属材料 )是一种新型无机非金属材料 |
B.多硫化合物(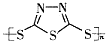 )化合物不能发生加成反应 )化合物不能发生加成反应 |
C.原电池的负极反应是将单体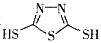 转化为 转化为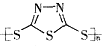 的过程 的过程 |
| D.当电路中有0.02mol电子通过时,原电池的负极将消耗原料0.46g |
气体的自动化检测中常常应用原电池原理的传感器。下图为电池的工作示意图:气体扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号。下表列出了待测气体及敏感电极上部分反应产物。则下列说法中正确的是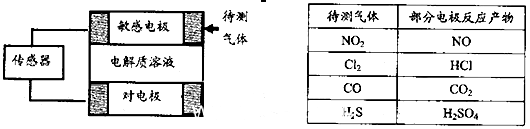
| A.上述气体检测时,敏感电极均作电池正极 |
B.检测Cl2气体时,敏感电极的电极反应为: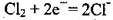 |
C.检测H2S气体时,对屯极充入空气,对电极上的电极反应式为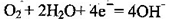 |
| D.检测H2S和CO体积分数相同的两份空气样本时,传感器上产生的电流大小相同 |
乙醛酸(OHCCOOH)是合成名贵高档香料乙基香兰素 的原料之一,可用草酸(HOOCCOOH)电解制备,装置如图所示。下列说法不正确的是( )
| A.电解时石墨电极应与直流电的正极相连 |
| B.阴极反应式为:HOOCCOOH+2H++2e-=OHCCOOH+H2O |
| C.电解时石墨电极上有O2放出 |
| D.电解一段时间后,硫酸溶液的pH不变化 |
原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关,下列说法中不正确的是( )
| A.由Al、Cu、稀H2SO4组成原电池,放电时SO42-向Al电极移动 |
| B.由Mg、Al、NaOH溶液组成原电池,其负极反应式为:Al-3e-+4OH-===AlO2-+2H2O |
| C.由Al、Cu、浓硝酸组成原电池作电源,用石墨电极来电解硝酸银溶液,当析出1 mol Ag时,消耗铜电极32 g |
| D.由Fe、Cu、FeCl3溶液组成原电池,其负极反应式为:Cu-2e-===Cu2+ |
把分别盛有熔融的氯化钾、氯化镁、氧化铝的三个电解槽串联,在一定条件下通电一段时间后,析出钾、镁、铝的物质的量之比为 ( )
| A.1︰2︰3 | B.3︰2︰1 | C.6︰3︰1 | D.6︰3︰2 |
一种太阳能电池的工作原理示意图如下所示,电解质为铁氰化钾K3[Fe(CN)6]和亚铁氰化钾K4[Fe(CN)6]的混合溶液,下列说法不正确的是( ) 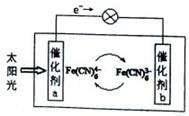
| A.K+移向催化剂b | B.催化剂a表面发生反应:Fe(CN)64――e-=Fe(CN)63- |
| C.Fe(CN)63-在催化剂b表面被氧化 | D.电解质溶液中Fe(CN)63-和Fe(CN)64-浓度基本保持不变 |
右图所示装置中,a、b、c、d、e、f均为惰性电极,电解质溶液均足量。接通电源后,d极附近显红色。下列说法正确的是
| A.电源B端是正极 |
| B.a、c电极均有单质生成,其物质的量之比为2:1 |
| C.欲用丁装置给铜镀银,N应为Ag,电解液为AgNO3溶液 |
| D.f极附近变红,说明氢氧化铁胶粒带正电荷 |