题目内容
1.下列有关能量变化和原因的相关叙述正确的是( )| A. | 反应是放热还是吸热,必须看反应物和生成物所具有的总能量的相对大小 | |
| B. | 铝热剂焊接钢轨主要利用的是光能 | |
| C. | 动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程 | |
| D. | Ba(OH)2•8H2O晶体与NH4Cl晶体的反应是放热反应 |
分析 A.化学反应的能量变化主要表现为放热或吸热,反应是放热还是吸热主要取决于反应物和生成物所具有的总能量的相对大小;
B.铝具有还原性,能用于冶炼金属;
C.葡萄糖被氧化成CO2是化学能转变成热能;
D.Ba(OH)2•8H2O晶体与NH4Cl晶体的反应是吸热反应.
解答 解:A.化学反应的能量变化主要表现为放热或吸热,反应是放热还是吸热主要取决于反应物和生成物所具有的总能量的相对大小,反应物的总能量大于生成物的总能量,则反应放热,反之吸热,故A正确;
B.铝具有还原性,能还原某些金属氧化物,铝热反应不能能还原氧化铁,且放出大量的热,所以利用铝与氧化铁发生的铝热反应来焊接钢轨,故B错误;
C.葡萄糖被氧化成CO2是化学能转变成热能,故C错误;
D.Ba(OH)2•8H2O晶体与NH4Cl晶体的反应是吸热反应,故D错误.
故选A.
点评 本题考查了能量转化与化学反应的方向问题,明确物质的性质是解本题关键,会运用化学知识解释生活现象,题目难度不大.

练习册系列答案
 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
11.海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程.下列有关说法正确的是
( )

( )

| A. | 用澄清的石灰水可鉴别NaHCO3和Na2CO3 | |
| B. | 溴元素在第③、⑤中被氧化,在第④中被还原 | |
| C. | 工业上一般用金属钠与无水MgCl2反应制取Mg单质 | |
| D. | 海水中还含有碘元素,只需将海水中的碘升华就可以得到碘单质 |
12.下列反应无论怎样调整反应物的用量,都只能生成一种物质的是( )
| A. | 甲烷与氯气混合后在光照的条件下发生反应 | |
| B. | 乙烯与水的加成反应 | |
| C. | 甲苯与浓硝酸发生硝化反应 | |
| D. | 2,3-二溴丁烷的消去反应 |
9.下列各组物质,用一种试剂无法区别的是( )
| A. | 三种浓酸:HNO3、H2SO4、HCl | |
| B. | 四种黑色粉末:FeO、Fe、CuO、C | |
| C. | 四种无色溶液:NaCl、NaOH、KOH、KCl | |
| D. | 四种白色粉末:(NH4)2SO4、NH4Cl、Na2SO4、NaCl |
16.某烃的结构简式为: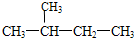 ,它的名称是( )
,它的名称是( )
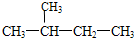 ,它的名称是( )
,它的名称是( )| A. | 3-甲基戊烷 | B. | 2,3-二甲基丙烷 | C. | 2-甲基丁烷 | D. | 3-甲基丁烷 |
13.假设体积可以相加,下列叙述中正确的是( )
| A. | pH=12的氨水,加水稀释100倍后溶液pH=10 | |
| B. | 90℃纯水的pH=6.2,则说明加热可导致水呈酸性 | |
| C. | 0.1mol•L-1的硫酸,与等体积水混合后溶液pH=1(假设混合后溶液的体积不变) | |
| D. | pH=3的盐酸与pH=11的氨水等体积混合后pH=7 |
10.在下列反应中,HCl作还原剂的是( )
| A. | Al2O3+6HCl=2AlCl3+3H2O | |
| B. | 2Al+6HCl=2AlCl3+3H2↑ | |
| C. | Al(OH)3+3HCl=AlCl3+3H2O | |
| D. | MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ MnCl2+Cl2↑+2H2O |
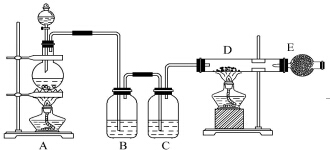
 实验室常采用点滴板来完成部分实验,这样既可以节约药品的用量,又便于观察实验现象.图中所示的实验,点滴板上描述的实验现象正确的是( )
实验室常采用点滴板来完成部分实验,这样既可以节约药品的用量,又便于观察实验现象.图中所示的实验,点滴板上描述的实验现象正确的是( )