题目内容
下列实验操作中错误的是
| A.蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 |
| B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| C.分液操作时,分液漏斗下层液体应从下口放出,上层液体应从上口倒出 |
| D.萃取操作时,所选萃取剂溶解溶质能力应大于原溶剂且与原溶剂互不相溶 |
A
解析试题分析:A、蒸发操作时,应使混合物中的水分接近蒸干时停止加热,利用余热完全蒸干,错误;B、蒸馏操作时,温度计测量的是蒸汽的温度,所以应使温度计水银球靠近蒸馏烧瓶的支管口处,正确;C、分液操作时,为了使液体彻底分离,分液漏斗下层液体应从下口放出,上层液体应从上口倒出,正确;D、萃取操作时,为了使溶质转移,所选萃取剂溶解溶质能力应大于原溶剂且与原溶剂互不相溶,正确。
考点:本题考查实验基本操作。

 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案以下是分析硫铁矿中FeS2含量的三种方法,各方法的操作流程图如下:
请回答下列问题:
(1)流程图中操作①、②、③分别指的是①_________、②__________、③________。
操作④、⑤用到的主要仪器是:④__________、⑤__________(每空填1-2个仪器)。
(2)判断溶液中SO42-离子已沉淀完全的方法是_________________________________。
(3)某同学用方法Ⅲ测定试样中Fe元素的含量,准确称取一定量的矿石试样,试样经溶解、预处理后,
| A.用带有刻度的烧杯配制成100 mL试样溶液。 | B.用量筒量取25.00 mL待测溶液, | C.并置于锥形瓶中。 | D.用蒸馏水洗涤滴定管后装入KMnO4标准溶液,用该标准溶液滴定待测试样,(E)当溶液变成淡紫红色时,停止滴定,如30秒内不褪色,(F)读取并计算滴定管中消耗的KMnO4标准溶液体积,计算试样中的Fe元素含量。请指出该实验过程中错误操作步骤的编号________________________。 |
(5)称取矿石试样1.60 g, 按方法Ⅰ分析,称得BaSO4的质量为4.66 g,假设矿石中的硫元素全部来自于FeS2,则该矿石中FeS2的质量分数是___________。
废旧物的回收利用既有利于节约资源,又有利于保护环境。某研究小组同学以废旧锌锰干电池为原料,将废旧电池含锌部分转化成ZnSO4·7H2O,含锰部分转化成纯度较高的MnO2,将NH4Cl溶液应用于化肥生产中,实验流程如下:
(1)操作②中所用的加热仪器应选 (选填“蒸发皿”或“坩埚”)。
(2)将溶液A处理的第一步是加入氨水调节pH为9,使其中的Fe3+和Zn2+沉淀,请写出氨水和Fe3+反应的离子方程式 。
(3)操作⑤是为了除去溶液中的Zn2+。已知25℃时,
| NH3·H2O的Kb | Zn2+完全沉淀的pH | Zn(OH)2溶于碱的pH |
| 1.8×10-5 | 8.9 | >11 |
由上表数据分析应调节溶液pH最好为 (填序号)。
a.9 b.10 c.11
(4) MnO2精处理的主要步骤:
步骤1:用3%H2O2和6.0mol/L的H2SO4的混和液将粗MnO2溶解,加热除去过量H2O2,得MnSO4溶液(含少量Fe3+)。反应生成MnSO4的离子方程式为 ;
步骤2:冷却至室温,滴加10%氨水调节pH为6,使Fe3+沉淀完全,再加活性炭搅拌,抽滤。加活性炭的作用是 ;
步骤3:向滤液中滴加0.5mol/L的Na2CO3溶液,调节pH至7,滤出沉淀、洗涤、干燥,灼烧至黑褐色,生成MnO2。灼烧过程中反应的化学方程式为 。
(5) 查文献可知,粗MnO2的溶解还可以用盐酸或者硝酸浸泡,然后制取MnCO3固体。
①在盐酸和硝酸溶液的浓度均为5mol/L、体积相等和最佳浸泡时间下,浸泡温度对MnCO3产率的影响如图4,由图看出两种酸的最佳浸泡温度都在 ℃左右;
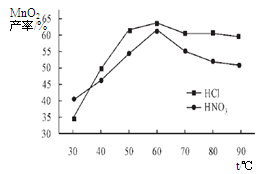
②在最佳温度、最佳浸泡时间和体积相等下,酸的浓度对MnCO3产率的影响如图5,由图看出硝酸的最佳浓度应选择 mol/L左右。

下列有关实验原理、方法和结论都正确的是
| A.向饱和FeCl3溶液中滴加过量氨水,可制取Fe(OH)3胶体 |
| B.取少量溶液X,向其中加入适量新制氨水,再加几滴KSCN溶液,溶液变红,说明X溶液中一定含有Fe2+ |
| C.室温下向苯和少量苯酚的混合溶液中加入适量NaOH溶液,振荡、静置后分液,可除去苯中少量苯酚 |
D.已知I3- I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大 I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大 |
下列实验操作中错误的是( )
| A.过滤操作时如果有必要可以用蒸馏水洗涤滤纸上的沉淀2-3次 |
| B.蒸馏操作时,应使温度计水银球插入液态混合物中 |
| C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D.萃取操作时,萃取剂要和原溶剂互不相溶,且不能与溶质和溶剂反应 |
为提纯下列物质(括号内为杂质),所选试剂及方法均正确的是
| 选项 | 物质 | 除杂试剂 | 方法 |
| A | 溴苯(溴) | CCl4 | 分液 |
| B | NH3(H2O) | 浓硫酸 | 洗气 |
| C | 乙烷(乙烯) | 溴水 | 洗气 |
| D | CO2(SO2) | Na2CO3饱和溶液 | 洗气 |
用分液漏斗可以分离的一组混合物是 ( )
| A.溴苯和水 | B.乙酸乙酯和乙酸 | C.溴乙烷和乙醇 | D.乙醇和水 |
下列与试验操作相关的描述中,正确的是
| A.制乙酸乙酯时,迅速将乙醇注入浓硫酸中 |
| B.在石油蒸馏装置中,将温度计水银球插入液面以下 |
| C.用铂丝蘸取少量KCl溶液置于火焰上灼烧,直接观察火焰颜色,检验K+的存在 |
| D.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
某未知溶液可能含Cl-、CO32-、Na+、SO42-、Al3+。将溶液滴在蓝色石蕊试纸上,试纸变红。取少量试液,滴加硝酸酸化的氯化钡溶液,有白色沉淀生成;在上层清液中滴加硝酸银溶液,产生白色沉淀。下列判断合理的是
| A.一定有Cl- | B.一定有SO42- | C.一定没有Al3+ | D.一定没有CO32- |