题目内容
【题目】下列反应中既是氧化还原反应又是吸热反应的是
A. 钾与水的反应
B. 灼热的木炭与CO2反应
C. 酒精的燃烧反应
D. Ba(OH)2·8H2O晶体与NH4Cl晶体的反应
【答案】B
【解析】A. 钾与水的反应既是氧化还原反应又是放热反应,A错误;B. 灼热的木炭与CO2反应既是氧化还原反应又是吸热反应,B正确;C. 酒精的燃烧反应既是氧化还原反应又是放热反应,C错误;D. Ba(OH)2·8H2O晶体与NH4Cl晶体的反应是吸热反应,但不是氧化还原反应,D错误,答案选B。

【题目】正溴丁烷(CH3CH2CH2CH2Br)是一种重要的有机合成工业原料。在实验中可利用下图装置(加热或夹持装置省略)制备正溴丁烷。
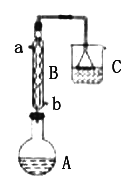
制备时的化学反应方程式及有关数据如下:NaBr+H2SO4(浓)===HBr+NaHSO4
C4H9OH+HBr![]() C4H9Br+H2O
C4H9Br+H2O
物质 | 相对分子质量 | 密度/g·cm-3 | 沸点/℃ | 水中溶解性 |
正丁醇 | 74 | 0.80 | 117.3 | 微溶 |
正溴丁烷 | 137 | 1.27 | 101.6 | 难溶 |
溴化氢 | 81 | --- | --- | 极易溶解 |
实验步骤:在装置A中加入2mL水,并小心加入28mL浓硫酸,混合均匀后冷却至室温。再依次加入18.5mL正丁醇和26g溴化钠,充分摇振后加入沸石,连接气体吸收装置C。将装置A置于石棉网上加热至沸腾,然后调节为小火使反应物保持平稳地回流。一段时间后停止加热,待反应液冷却后,拆去装置B,改为蒸馏装置,蒸出粗正溴丁烷。
请回答下列问题;
(1)仪器A的名称是________;仪器B的作用是______。
(2)装置C中盛装的液体是________;其作用是_________ 。
(3)制备的粗产物正溴丁烷中往往含有水分、正丁醇等杂质,加入干燥剂出去水分后,再由下列操作中的________制备纯净的正溴丁烷。
A.分液 B.萃取 C.重结晶 D.蒸馏
(4)若制备实验的“回流”过程中不采用“调节为小火”,仍采用大火加热回流,则会使产品产率偏_________(填“高”或“低”),试说出其中一种原因:__________________________________________________。
(5)若最终得到13.6g纯净的正溴丁烷,则该实验的产率是___________(保留三位有效数字)。