题目内容
【题目】合理利用或转化NO2、SO2、CO、NO等污染性气体是人们共同关注的课题。
Ⅰ.某化学课外小组查阅资料后得知:2NO(g)+O2(g)![]() 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:
①2NO(g)![]() N2O2(g)(快) v1正=k1正·c2(NO),v1逆=k1逆·c(N2O2) H1<0
N2O2(g)(快) v1正=k1正·c2(NO),v1逆=k1逆·c(N2O2) H1<0
②N2O2(g)+O2(g)![]() 2NO2(g)(慢) v2正=k2正·c(N2O2)·c(O2),v2逆=k2逆·c2(NO2) H2<0
2NO2(g)(慢) v2正=k2正·c(N2O2)·c(O2),v2逆=k2逆·c2(NO2) H2<0
请回答下列问题:

(1)反应2NO(g)+O2(g)![]() 2NO2(g)的H=________________(用含H1和H2的式子表示)。一定温度下,反应2NO(g)+O2(g)
2NO2(g)的H=________________(用含H1和H2的式子表示)。一定温度下,反应2NO(g)+O2(g)![]() 2NO2(g)达到平衡状态,写出用k1正、k1逆、k2正、k2逆表示平衡常数的表达式K=_____________________。
2NO2(g)达到平衡状态,写出用k1正、k1逆、k2正、k2逆表示平衡常数的表达式K=_____________________。
(2)决定2NO(g)+O2(g)![]() 2NO2(g)反应速率是反应②,反应①的活化能E1与反应②的活化能E2的大小关系为E1________E2(填“>”、“<”或“=”)。
2NO2(g)反应速率是反应②,反应①的活化能E1与反应②的活化能E2的大小关系为E1________E2(填“>”、“<”或“=”)。
Ⅱ.(3)反应N2O4(g)![]() 2NO2(g),在一定条件下N2O4与NO2的消耗速率与自身压强有如下关系:v(N2O4)=k1·p(N2O4),v(NO2)=k2·p2(NO2)。其中k1、k2是与温度有关的常数。一定温度下,相应的速率与压强关系如图所示,在图中标出的点中,能表示该反应达到平衡状态的两个点是_______________,理由是__________________________________________________________________________________________。
2NO2(g),在一定条件下N2O4与NO2的消耗速率与自身压强有如下关系:v(N2O4)=k1·p(N2O4),v(NO2)=k2·p2(NO2)。其中k1、k2是与温度有关的常数。一定温度下,相应的速率与压强关系如图所示,在图中标出的点中,能表示该反应达到平衡状态的两个点是_______________,理由是__________________________________________________________________________________________。
(4)在25℃时,将a mol·L-1的氨水溶液与0.02 mol·L-1 HCl溶液等体积混合后溶液恰好呈中性(忽略溶液混合后体积的变化),用含a的表达式表示250C时NH3·H2O的电离常数Kb=_________________。用质量分数为17%,密度为0.93 g/cm3的氨水,配制200 mL a mol·L-1的氨水溶液,所需原氨水的体积V=___________mL。
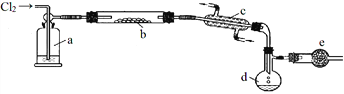
(5)如图电解装置可将雾霾中的NO、SO2分别转化为NH4+和SO42-。物质A的化学式为_________,阴极的电极反应式是__________________________。

【答案】 △H1+△H2 ![]() < BD 图中只有D点NO2的消耗速率是B点N2O4的消耗速率的2倍,所以表示达到化学平衡状态的点是BD (2×10-9 )/(a-0.02) 21.5a或200a/9.3或2000a/93 H2SO4 NO+6H++5e-=NH4++H2O
< BD 图中只有D点NO2的消耗速率是B点N2O4的消耗速率的2倍,所以表示达到化学平衡状态的点是BD (2×10-9 )/(a-0.02) 21.5a或200a/9.3或2000a/93 H2SO4 NO+6H++5e-=NH4++H2O
【解析】Ⅰ.(1)①2NO(g)N2O2(g);②N2O2(g)+O2(g)2NO2(g),而目标反应2NO(g)+O2(g)2NO2(g)的△H=①+②=△H1+△H2,由反应达平衡状态,所以v1正=v1逆、v2正=v2逆,所以v1正×v2正=v1逆×v2逆,即k1正c2(NO)×k2正c(N2O2)c(O2)=k1逆c(N2O2)×k2逆c2(NO2),则是K=![]() ;
;
(2)因为决定2NO(g)+O2(g)2NO2(g)速率的是反应②,所以反应①的活化能E1远小于反应②的活化能E2;
II .(3)满足平衡条件υ(NO2)=2υ(N2O4)即为平衡点,B、D点的压强之比等于其反应速率之比为1:2,所以B、D为平衡点;
(3)反应后溶液中c(NH4+)=c(Cl-)=0.01mol/L,c(NH3H2O)=![]() mol/L-c(NH4+)=
mol/L-c(NH4+)=![]() mol/L,c(OH-)=10-7mol/L,则Kb=
mol/L,c(OH-)=10-7mol/L,则Kb=![]() =
= =(2×10-9 )/(a-0.02);设氨水的体积为VmL,则根据稀释定律可知:V×0.93g·cm-3×17%=amol·L-1×0.2L,解得V=21.5a mL。
=(2×10-9 )/(a-0.02);设氨水的体积为VmL,则根据稀释定律可知:V×0.93g·cm-3×17%=amol·L-1×0.2L,解得V=21.5a mL。
(4)NO得电子生成铵根,离子方程式为NO+5e-+6H+=NH4++H2O,为阴极反应,阳极上SO2失电子形成硫酸。

 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案