题目内容
同一周期元素,其原子结构相同之处是( )
| A、最外层电子数相等 |
| B、核电荷数相等 |
| C、电子层数相等 |
| D、核外电子数相等 |
考点:元素周期表的结构及其应用
专题:元素周期律与元素周期表专题
分析:同一周期元素,电子层相同,最外层电子数不同,以此来解答.
解答:
解:A.同周期元素的最外层电子数不同,从左向右增大,故A不选;
B.同周期,原子的核电荷数从左向右增大,故B不选;
C.原子结构中,电子层数=周期数,则同一周期元素的电子层数相等,故C选;
D.核外电子数=核电荷数,同周期,原子的核电荷数从左向右增大,故D不选;
故选C.
B.同周期,原子的核电荷数从左向右增大,故B不选;
C.原子结构中,电子层数=周期数,则同一周期元素的电子层数相等,故C选;
D.核外电子数=核电荷数,同周期,原子的核电荷数从左向右增大,故D不选;
故选C.
点评:本题考查元素周期表的结构及应用,明确原子结构与元素位置的关系为解答的关键,注意电子层数=周期数即可解答,题目难度不大.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
已知短周期元素的离子,a A2+、b B+、c C3+、d D-都具有相同的电子层结构,则下列叙述正确的是( )
| A、原子半径:A>B>D>C |
| B、原子序数:c>a>b>d |
| C、离子半径:C>D>B>A |
| D、单质的还原性:A>B>D>C |
对于反应3Cl2+6NaOH
5NaCl+NaClO3+3H2O,以下叙述正确的是( )
| ||
| A、Cl2是氧化剂,NaOH是还原剂 |
| B、当有6.72L Cl2反应时,转移电子物质的量为0.5mol |
| C、氧化剂得电子总数与还原剂失电子总数之比为1:1 |
| D、被氧化的氯原子和被还原的氯原子的物质的量之比为5:1 |
下列几种物质均能使品红褪色,其中有一种物质使品红褪色的原理与其他几种不同,该物质是( )
| A、二氧化硫 | B、臭氧 |
| C、次氯酸 | D、次氯酸钠 |
以下化学用语不正确的是( )
| A、乙炔的最简式 CH |
B、CH4的球棍模型: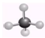 |
| C、乙烯的结构简式CH2CH2 |
| D、乙醇的结构简式C2H5OH |
下列实验能达到实验目的是( )
| A、用100mL容量瓶量取50mL水 |
| B、用四氯化碳萃取碘水中的碘 |
| C、用浓硫酸干燥氨气 |
| D、用pH试纸测定氯水的pH |
下列离子方程式正确的是( )
| A、常温下,将铁片置于过量的浓硝酸中:Fe+6H++3NO3-═Fe3++3NO2↑+3H2O | ||||
B、加热条件下,铜与浓硫酸反应:4H++SO42-+Cu
| ||||
| C、常温下,向(NH4)2SO4溶液中加入适量Ba(OH)2:Ba2++SO42-═BaSO4↓ | ||||
| D、常温下,向稀硝酸中加入过量的铁片:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O |