题目内容
【题目】下列事实不能用勒夏特列原理来解释的是
A. 用排饱和食盐水的方法收集氯气
B. 加入催化剂使N2和H2在一定条件下生成氨气
C. 增大压强,有利于SO2和O2反应生成SO3
D. 在Fe3+ + 3SCN- ![]() Fe(SCN)3反应达平衡时,增加KSCN的浓度,体系颜色变深
Fe(SCN)3反应达平衡时,增加KSCN的浓度,体系颜色变深
【答案】B
【解析】
A.用排饱和食盐水的方法收集氯气,相当于在氯水中加入NaCl,c(Cl-)增大,反应Cl2+H2O![]() H++Cl-+HClO的平衡左移,减小了氯气的溶解度,能用勒夏特列原理解释,故不选A;
H++Cl-+HClO的平衡左移,减小了氯气的溶解度,能用勒夏特列原理解释,故不选A;
B.加入催化剂使N2和H2在一定条件下生成氨气,利用催化剂增大反应速率,催化剂不会引起化学平衡的移动,不能用勒夏特列原理解释,故选B;
C.增大压强,反应2SO2+O2![]() 2SO3的平衡右移,能用勒夏特列原理解释,故不选C;
2SO3的平衡右移,能用勒夏特列原理解释,故不选C;
D.在Fe3+ + 3SCN-![]() Fe(SCN)3反应达平衡时,增加KSCN的浓度,平衡右移,体系颜色变深,能用勒夏特列原理解释,故不选D;
Fe(SCN)3反应达平衡时,增加KSCN的浓度,平衡右移,体系颜色变深,能用勒夏特列原理解释,故不选D;
本题答案为B。

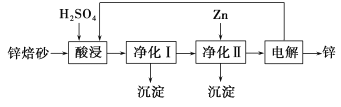
【题目】ⅥA族元素形成的化合物在实验室和工业生产上有着广泛的应用。回答下列问题:
(1)SCN-与Fe3+可形成多种配离子,其中一种为[Fe(SCN)6]3-,该配离子中的SCN-会使Fe3+的剩余价电子压缩配对,则每个配离子中Fe3+的单电子个数为_________个。
(2)Se与S是同族元素,请写出基态Se原子电子排布式_____________。H2Se的酸性比H2S________(填“强”或“弱”)。H2O、H2S、H2Se沸点由高到低的顺序为__________________,原因是:___________。
(3)有一种由1~9号元素中的部分元素组成,且与SCl2互为等电子体的共价化合物,它的分子式为_______,其VSEPR构型为_____________。
(4)已知S4O62-的结构为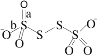 ,其中S原子的杂化方式是_______________。键长a______b(填“>”、“<”或“=”)。
,其中S原子的杂化方式是_______________。键长a______b(填“>”、“<”或“=”)。
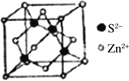
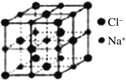
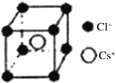
(5)离子晶体中阳离子和阴离子的半径比不同可形成不同的晶胞结构,见下表:
半径比 | 0.225~0.414 | 0.414~0.732 | 0.732~1 |
典型化学式 | 立方ZnS | NaCl | CsCl |
晶胞 |
|
|
|
已知某离子晶体RA,其阴阳离子半径分别为184pm和74pm,摩尔质量为M g/mol,则阳离子配位数为___________,晶体的密度为_________g/cm3(列出计算式,无需化简,设NA为阿伏加德罗常数的值)。