��Ŀ����
����Ŀ������Ա����������CO2�����з�Ӧ��������ʵ�ֿռ�վ��O2��ѭ�����á�
Sabatier��Ӧ��CO2(g)+4H2(g)![]() CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
ˮ��ⷴӦ��2H2O(l) ![]() 2H2(g) + O2(g)
2H2(g) + O2(g)
��1����ԭ������![]() ��
��![]() =1��4�����ܱ������з���Sabatier��Ӧ�����H2O(g)�����ʵ����������¶ȵĹ�ϵ��ͼ��ʾ�����߱�ʾƽ�����ߣ���
=1��4�����ܱ������з���Sabatier��Ӧ�����H2O(g)�����ʵ����������¶ȵĹ�ϵ��ͼ��ʾ�����߱�ʾƽ�����ߣ���
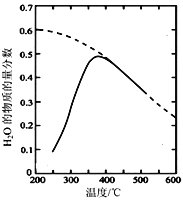
�� �÷�Ӧ��ƽ�ⳣ��K���¶����߶�__________�������С������
�� �¶ȹ�����;������ڸ÷�Ӧ�Ľ��У�ԭ����__________________________��
�� 200��ﵽƽ��ʱ��ϵ����ѹǿΪp���÷�Ӧƽ�ⳣ��Kp�ļ���ʽΪ________�������ػ�����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ����ѹ�����ʵ���������
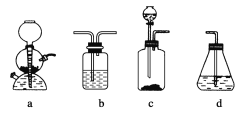
��2��Sabatier��Ӧ�ڿռ�վ����ʱ�����д�ʩ�����CO2ת���ʵ���______�����ţ���
A���ʵ���ѹ B����������ıȱ����
C����Ӧ��ǰ�μ��ȣ������ȴ D�����ԭ������H2��ռ����
��3��һ���µ�ѭ�����÷�������Bosch��ӦCO2(g)+2H2(g)![]() C(s)+2H2O(g)����Sabatier��Ӧ��
C(s)+2H2O(g)����Sabatier��Ӧ��
�� ��֪CO2(g)��H2O(g)�������ʷֱ�Ϊ�C394 kJmol��1���C242 kJmol��1��Bosch��Ӧ�Ħ�H ��________kJmol��1����������ָһ���������ɶ�Ӧ��������1mol������ʱ�ķ�Ӧ�ȣ�
�� һ��������Bosch��Ӧ�����ڸ����²���������ԭ����______________________��
���𰸡� ��С �¶ȹ��ͣ���Ӧ����С���¶ȹ��ߣ���Ӧ���ҽ��еij̶�С�����¶ȹ��ߣ���Ӧ������У�  CD -90 ��Ӧ�Ļ�ܸ�
CD -90 ��Ӧ�Ļ�ܸ�
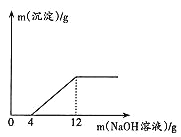
����������1���ٸ���ͼ��ƽ��ʱˮ�����ʵ��������������¶ȵ����߶���С����֪�÷�Ӧ����ӦΪ���ȷ�Ӧ��ƽ�ⳣ�����¶ȵ����߶���С����ȷ������С��
�ڷ�Ӧ�������¶ȵ����߶������¶ȹ��ͣ����ʽ�С����Ӧ���л������÷�ӦΪ���ȷ�Ӧ���¶ȹ��ߣ�ƽ�����ƣ������ڷ�Ӧ�Ľ��У���ȷ�𰸣��¶ȹ��ͣ���Ӧ����С���¶ȹ��ߣ���Ӧ���ҽ��еij̶�С�����¶ȹ��ߣ���Ӧ������У���
�� ����ͼ���֪��200��ʱ��Ӧ�ﵽƽ��ʱˮ�����ʵ�������0.1��ƽ��ʱˮ��ռ��ѹǿΪ0.6p�����ݻ�ѧ����ʽ��֪������ռ��ѹǿΪ0.3 p����˶�����̼��������ռ��ѹǿΪ0.1p�����ݳ�ʼͶ�ϱ��Լ�������̼�������Ļ�ѧ������֮�ȿ�֪��Ӧ�ﵽƽ��ʱ�����ߵ����ʵ���֮��ҲΪ1:4����ƽ��ʱ������̼��ռ��ѹǿΪ0.02p��������ռ��ѹǿΪ0.08 p�����Ը÷�Ӧƽ�ⳣ��Kp�ļ���ʽΪ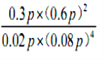 ����ȷ�𰸣�
����ȷ�𰸣�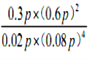 ��
��
��2���÷�ӦΪһ�������С���淴Ӧ����Сѹǿ��ƽ�����ƣ�CO2ת���ʽ��ͣ�A������������ıȱ�����������˴����뷴Ӧ��ĽӴ������������ߴ����Ĵ�Ч�ʣ��ӿ췴Ӧ���ʣ�����ƽ�ⲻ�ƶ���ת���ʲ��䣬B����Ӧ��ǰ�μ��ȣ����Լӿ췴Ӧ�����ʣ������ȴ���Լ���������ˮ������Ũ�ȣ�ƽ�����ƣ����CO2ת���ʣ�C��ȷ�����ԭ������H2��ռ������������CO2ת���ʣ�D��ȷ����ȷѡ��CD��
��3���ٸ������������֪��C(s)+O2(g)==CO2(g) ��H=�C394 kJmol��1,H2(g)+1/2O2(g)= H2O(g) ��H=�C242 kJmol��1,�ڶ�����Ӧ��2-��һ����Ӧ�ɵ�CO2(g)+2H2(g)![]() C(s)+2H2O ��H ��-90 kJmol��1����ȷ�𰸣�-90��
C(s)+2H2O ��H ��-90 kJmol��1����ȷ�𰸣�-90��
���ڻ�ѧ��Ӧ�У�ֻ�л���Ӳ��ܷ�����Ч��ײ��������ѧ��Ӧ�����¿�����߷�Ӧ�Ļ�ܣ��Ӷ����ڷ�Ӧ�ķ��������÷�Ӧ�ķ�Ӧ��ܸߣ������ڸ����²�����������ȷ�𰸣���Ӧ�Ļ�ܸߡ�

 ÿ�α���ϵ�д�
ÿ�α���ϵ�д�