题目内容
【题目】取盐酸与氯化铜的混合溶液27g放入烧杯中,逐滴滴入质量分数为20%的氢氧化钠溶液,产生沉淀质量与滴入氢氧化钠溶液质量关系如图所示。
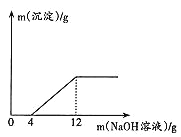
(1)滴入氢氧化钠溶液的质量在0~4g时,发生反应的化学方程式为___________。
(2)与氯化铜反应的氢氧化钠的质量为____________g。
(3)求原盐酸与氯化铜的混合溶液中氯化铜的质量分数______(写出计算过程)。
【答案】NaOH+HCl=NaCl+H2O1.6g10%
【解析】
(1)从图象可以看出,滴入NaOH溶液的质量在0~4g时,没有出现沉淀,所以是盐酸和氢氧化钠的反应,盐酸和氢氧化钠反应生成氯化钠和水,化学方程式为HCl+NaOH=NaCl+H2O;
(2)从图象中的数据可以看出,从加入氢氧化钠4g开始出现沉淀,到加入氢氧化钠12g,沉淀开始不变,所以与氯化铜反应的NaOH的质量为(12-4)g×20%=1.6g;
(3)设原盐酸与氯化铜的混合溶液中氯化铜的质量为x g,则根据方程式可知
CuCl2+2NaOH=Cu(OH)2↓+2NaCl
135 80
x 1.6g
则
135:80=x:1.6g
解得x=2.7g
所以原盐酸与氯化铜的混合溶液中氯化铜的质量分数为2.7g÷27g×100%=10%。

练习册系列答案
相关题目






