题目内容
14.有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同.下列各项的事实不能说明上述观点的是( )| A. | 甲苯能使酸性高锰酸钾溶液褪色,而甲烷不能使酸性高锰酸钾溶液褪色 | |
| B. | 乙醛能与氢气加成,而乙酸不能与氢气加成 | |
| C. | 乙醇能与金属钠反应,而甲醚不能与金属钠反应 | |
| D. | 苯酚能与NaOH溶液反应,而乙醇不能与NaOH溶液反应 |
分析 A.甲基连接在苯环上,可被氧化;
B.羟基对羰基的影响;
C.乙醇与甲醚无相同的官能团;
D.苯环对酚羟基影响的结果是酚羟基具有酸性.
解答 解:A.甲基连接在苯环上,可被氧化,说明苯环对甲基影响,故A不选;
B.乙醛和乙酸都含有羰基,乙醛能与氢气加成,而乙酸不能与氢气加成,说明乙酸分子中-OH对羰基的影响,故B不选;
C.乙醇中含有-OH,能与钠反应,而甲醚中无此结构,不能与金属钠反应,不能用上述观点证明,故C选;
D.在苯酚中,由于苯环对-OH的影响,酚羟基具有酸性,对比乙醇,虽含有-OH,但不具有酸性,能说明上述观点,故D不选;
故选C.
点评 本题考查有机物的结构与性质关系,题目难度不大,关键根据原子团所处的化学环境进行比较性质差异,并熟悉官能团与物质性质的关系来解答.

练习册系列答案
相关题目
4.如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法正确的是( )


| A. | 该硫酸的物质的量浓度为9.2 mol•L-1 | |
| B. | 1 mol 铁加入到足量的该硫酸中,可产生2 g H2 | |
| C. | 该硫酸与等质量的水混合所得溶液的物质的量浓度大于9.2 mol•L-1 | |
| D. | 配制200 mL 4.6 mol•L-1的硫酸溶液需取该硫酸50 mL |
2.有两种气态不饱和烃的混合物共20mL,完全燃烧可生成H2O蒸气72mL和CO276mL(气体体积均在同温同压下测定),则这两种烃的分子式为( )
| A. | C2H4、C4H8 | B. | C2H2、C3H8 | C. | C3H4、C4H8 | D. | C3H4、C3H8 |
19.某溶液仅含Fe2+、Na+、Al3+、Ba2+、SO42-、CO32-、HCO3-、NO3-、Cl-中的4种离子,所含离子的物质的量均为1mol.若向该溶液中加入少量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解).下列说法不正确的是( )
| A. | 若向该溶液中加入过量的稀硫酸,溶液中阴离子种类仍不变 | |
| B. | 若向该溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为72g | |
| C. | 若向该溶液中加入过量的稀硫酸和KSCN溶液,溶液显血红色 | |
| D. | 该溶液中一定不含Al3+、Ba2+、Cl- |
3.下列反应的离子方程式正确的是( )
| A. | 过量二氧化碳通入偏铝酸钠溶液中:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- | |
| B. | 在溶液中亚硫酸氢铵与等物质的量氢氧化钠混合:NH4++HSO3-+2OH-═SO32-+NH3↑+2H2O | |
| C. | 氯气通入冷的烧碱溶液中:2Cl2+2OH-═3Cl-+ClO-+H2O | |
| D. | 碳酸氢镁溶液中加入过量的石灰水:Mg2++2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+MgCO3↓ |
16.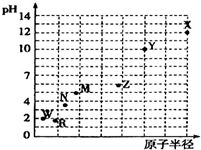 第三周期元素的最高价氧化物对应水化物(浓度均为0.01mol•L-1)的pH值与原子半径的关系如图所示,则下列说法正确的是( )
第三周期元素的最高价氧化物对应水化物(浓度均为0.01mol•L-1)的pH值与原子半径的关系如图所示,则下列说法正确的是( )
 第三周期元素的最高价氧化物对应水化物(浓度均为0.01mol•L-1)的pH值与原子半径的关系如图所示,则下列说法正确的是( )
第三周期元素的最高价氧化物对应水化物(浓度均为0.01mol•L-1)的pH值与原子半径的关系如图所示,则下列说法正确的是( )| A. | 气态氢化物的稳定性:R>W | |
| B. | Z的最高价氧化物对应的水化物能溶于稀氨水 | |
| C. | Y的单质是制造汽车、飞机、火箭的重要材料 | |
| D. | 简单离子的半径X的最大 |
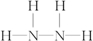 ,1mol戊与过量盐酸反应的离子方程式是N2H4+2H+═N2H62+ 戊在氧化还原反应中与H2O2相似,既可作氧化剂,又可作还原剂,根据价态分析产生这种情况的原因是N2H4中氮元素的化合价为-2价,既可以升高,又可以降低;8g液态戊与液态双氧水恰好完全反应,产生两种无毒又不污染环境的气态物质,放出375kJ的热量,写出该反应的热化学方程式N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-1 500 kJ/mol.
,1mol戊与过量盐酸反应的离子方程式是N2H4+2H+═N2H62+ 戊在氧化还原反应中与H2O2相似,既可作氧化剂,又可作还原剂,根据价态分析产生这种情况的原因是N2H4中氮元素的化合价为-2价,既可以升高,又可以降低;8g液态戊与液态双氧水恰好完全反应,产生两种无毒又不污染环境的气态物质,放出375kJ的热量,写出该反应的热化学方程式N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-1 500 kJ/mol.