题目内容
【题目】如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准).则下列有关说法正确的是( )
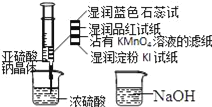
A. 湿润淀粉碘化钾试纸未变蓝说明硫元素的非金属性强于碘元素
B. 沾有KMnO4溶液的滤纸褪色证明了SO2具有漂白性
C. 实验后,可把注射器中的物质缓缓推入NaOH溶液中,以减少环境污染
D. 蓝色石蕊试纸变红说明SO2显酸性
【答案】C
【解析】
A.湿润淀粉KI试纸未变蓝,说明SO2不能将KI氧化为I2,不能说明硫元素的非金属性强于碘元素,A错误;
B.SO2具有还原性,与具有强氧化性的KMnO4发生氧化还原反应,表现出SO2的还原性,而不是漂白性,B错误;
C.SO2为酸性气体,有毒,可与NaOH溶液反应生成盐和水,所以NaOH溶液可用于除去实验中多余的SO2,C正确;
蓝色石蕊试纸变红说明SO2与水反应产生的物质显酸性,D错误;
故合理选项是C。

【题目】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=___。
(2)该反应为___反应(选填吸热、放热)。
(3)能判断该反应是否达到化学平衡状态的依据是___(多选扣分)。
a.υ正(H2)=υ逆(H2O) b.反应停止,正、逆反应速率都等于零
c.容器中压强不再发生变化 d.混合气体中c(CO2)不变
(4)某温度下,在2L的密闭容器中,加入1 molCO2和1molH2充分反应达平衡时,CO平衡浓度为0.25mol/L,试判断此时的温度为__℃。
(5)若在(4)所处的温度下,在1L的密闭容器中,加入2molCO2和3molH2充分反应达平衡时,CO2的平衡转化率为___。