题目内容
【题目】按要求写出下列反应的化学方程式或离子方程式:
(1)Na和H2O反应的离子方程式___________________ ;
(2) Al2O3和NaOH反应的离子方程式___________________ ;
(3)Al和NaOH溶液反应的离子方程式___________________ ;
(4)Na2O2和CO2反应的化学方程式___________________ ;
(5) NaHCO3受热分解的化学方程式___________________ ;
(6)Fe与水蒸气在高温下反应化学方程式___________________ ;
【答案】2Na+2H2O===2Na++2OH-+H2↑ Al2O3+2OH-===2AlO2-+H2O 2Al+2OH-+2H2O===2AlO2-+3H2↑ 2Na2O2+2CO2===2Na2CO3+O2 2NaHCO3![]() Na2CO3+CO2↑+H2O 3Fe+4H2O(g)
Na2CO3+CO2↑+H2O 3Fe+4H2O(g) ![]() Fe3O4+4H2
Fe3O4+4H2
【解析】
(1)钠与水反应生成氢氧化钠和氢气;
(2)Al2O3与NaOH溶液反应生成偏铝酸钠和水;
(3)铝与氢氧化钠溶液反应生成偏铝酸钠和氢气;
(4)Na2O2和CO2反应生成碳酸钠和氧气;
(5)NaHCO3受热分解生成碳酸钠和二氧化碳;
(6)Fe与水蒸气在高温下反应生成四氧化三铁和氢气。
(1)钠与水反应生成氢氧化钠和氢气,反应的离子方程式为:2Na+2H2O=2Na++2OH-+H2↑;故答案为:2Na+2H2O===2Na++2OH-+H2↑;
(2)Al2O3与NaOH溶液反应生成偏铝酸钠和水,反应的离子方程式是:Al2O3+2OH-=2AlO2-+H2O,故答案为:Al2O3+2OH-===2AlO2-+H2O;
(3)铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,反应的化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,故答案为:2Al+2NaOH+2H2O===2NaAlO2+3H2↑;
(4)Na2O2和CO2反应生成碳酸钠和氧气,化学方程式为:2Na2O2+2CO2===2Na2CO3+O2,故答案为:2Na2O2+2CO2===2Na2CO3+O2;
(5)NaHCO3受热分解生成碳酸钠和二氧化碳,化学方程式为:2NaHCO3![]() Na2CO3+CO2↑+H2O,故答案为:2NaHCO3
Na2CO3+CO2↑+H2O,故答案为:2NaHCO3![]() Na2CO3+CO2↑+H2O;
Na2CO3+CO2↑+H2O;
(6)Fe与水蒸气在高温下反应生成四氧化三铁和氢气,方程式为:3Fe+4H2O(g) ![]() Fe3O4+4H2,故答案为:3Fe+4H2O(g)
Fe3O4+4H2,故答案为:3Fe+4H2O(g) ![]() Fe3O4+4H2。
Fe3O4+4H2。

 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案【题目】化工原料异丁烯(C4H8)可由异丁烷(C4H10)直接催化脱氢制备:C4H10(g) ![]() C4H8(g) + H2(g)ΔH=+139 kJ/mol
C4H8(g) + H2(g)ΔH=+139 kJ/mol
(1)该反应的化学平衡常数的表达式为_________________。
(2)一定条件下,以异丁烷为原料生产异丁烯。温度、压强改变对异丁烷平衡转化率的
影响如下图所示。
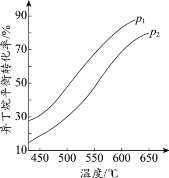
①判断p1、p2的大小关系:p1_________________(填“>”或“<”)p2,理由是_________________。
②若异丁烷的平衡转化率为40%,则平衡混合气中异丁烯的物质的量分数最多为______%(保留小数点后1位)。
(3)目前,异丁烷催化脱氢制备异丁烯的研究热点是催化活性组分以及载体的选择。下表是以V-Fe-K-O为催化活性物质,反应时间相同时,测得的不同温度、不同载体条件下的数据。
温度/℃ | 570 | 580 | 590 | 600 | 610 | |
以γ-Al2O3为载体 | 异丁烷转化率/% | 36.41 | 36.49 | 38.42 | 39.23 | 42.48 |
异丁烯收率/% | 26.17 | 27.11 | 27.51 | 26.56 | 26.22 | |
以TiO2为载体 | 异丁烷转化率/% | 30.23 | 30.87 | 32.23 | 33.63 | 33.92 |
异丁烯收率/% | 25.88 | 27.39 | 28.23 | 28.81 | 29.30 | |
说明:收率=(生产目标产物的原料量/原料的进料量)×100%
①由上表数据,可以得到的结论是____________(填字母序号)。
a.载体会影响催化剂的活性
b. 载体会影响催化剂的选择性
c.载体会影响化学平衡常数
②分析以γ-Al2O3为载体时异丁烯收率随温度变化的可能原因:___________。