题目内容
【题目】某溶液A中可能只含有Fe3+、Fe2+、Ag+、Mg2+、Al3+、NH4+、Cl-、NO3—、SO42—中的若干种离子,为确认其中含有的各离子,取1 L溶液A,进行如下所示实验:
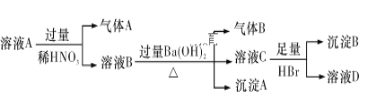
已知:气体A、气体B的体积都为2.24 L(标准状况下),沉淀B的物质的量为0.1 mol。根据以上实验操作与现象,判断下列说法错误的是( )
A. 溶液A中一定含有Fe2+、NH4+、Ag+、NO3—,一定不含Cl-、SO42—
B. 沉淀A中一定含有Fe(OH)3,可能含有Mg(OH)2 、Al(OH)3
C. 溶液D中可能含有Al3+
D. 溶液A中的c(NO3—)≥1.0 mol/L
【答案】B
【解析】
溶液A能与过量的稀硝酸反应,生成气体A,说明溶液A中含有还原性离子,即含有Fe2+,气体A的体积为2.24L,根据得失电子数目守恒,得出n(Fe2+)=2.24×3/22.4mol=0.3mol,溶液B中加入过量Ba(OH)2溶液,并加热,有气体B产生,即该气体为NH3,说明原溶液中含有NH4+,n(NH3)=0.1mol,沉淀A中一定含有Fe(OH)3,溶液C加入足量的HBr,生成沉淀B,沉淀B为AgBr,原溶液中一定含有Ag+,沉淀B的物质的量为0.1mol,则原溶液中Ag+的物质的量为0.1mol,产生的NH3能与Ag+反应生成[Ag(NH3)2]+,得出NH3总物质的量为(0.1+0.1×2)mol=0.3mol,即原溶液中n(NH4+)=0.3mol,根据离子共存,可以得出原溶液中一定不含有的离子是SO42-、Cl-,溶液呈现电中性,原溶液中一定存在NO3-;
溶液A能与过量的稀硝酸反应,生成气体A,说明溶液A中含有还原性离子,即含有Fe2+,气体A的体积为2.24L,根据得失电子数目守恒,得出n(Fe2+)=2.24×3/22.4mol=0.3mol,溶液B中加入过量Ba(OH)2溶液,并加热,有气体B产生,即该气体为NH3,说明原溶液中含有NH4+,n(NH3)=0.1mol,沉淀A中一定含有Fe(OH)3,溶液C加入足量的HBr,生成沉淀B,沉淀B为AgBr,原溶液中一定含有Ag+,沉淀B的物质的量为0.1mol,则原溶液中Ag+的物质的量为0.1mol,产生的NH3能与Ag+反应生成[Ag(NH3)2]+,得出NH3总物质的量为(0.1+0.1×2)mol=0.3mol,即原溶液中n(NH4+)=0.3mol,根据离子共存,可以得出原溶液中一定不含有的离子是SO42-、Cl-,溶液呈现电中性,原溶液中一定存在NO3-;
A、根据上述分析,原溶液中一定含有Fe2+、NH4+、Ag+、NO3-,一定不含有的离子是SO42-、Cl-,可能存在的离子是Fe3+、Mg2+、Al3+,故A说法正确;
B、因为Ba(OH)2是过量,氢氧化铝表现两性,即沉淀A中不含氢氧化铝,故B说法错误;
C、根据上述分析,溶液D中可能含有Al3+,故C说法正确;
D、根据上述分析,原溶液中NO3-至少物质的量为(0.3×2+0.3+0.1)mol=1.0mol,原溶液可能含有Fe3+、Mg2+、Al3+,因此c(NO3-)至少为1.0/1mol·L-1=1.0mol·L-1,故D说法正确。