题目内容
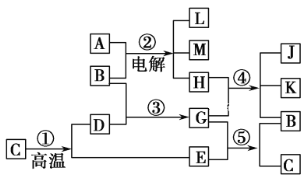
【题目】工业上用铝土矿(含氧化铝、氧化铁)制取铝的过程如下:
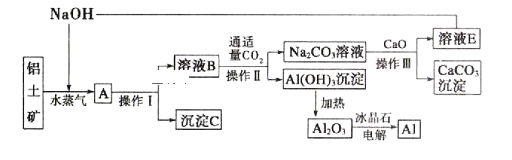
请回答下列问题。
(1)沉淀C的化学式为_______________,该物质除了用于金属冶炼以外,还可用作____________。
(2)电解熔融的氧化铝时,若得到22.4L(标准状况下)![]() ,则同时生成___________g铝。
,则同时生成___________g铝。
(3)操作I、操作II和操作III都是__________(填操作名称),实验室要洗涤,![]() 沉淀应该在____________装置中进行,洗涤方法是_____________________________。
沉淀应该在____________装置中进行,洗涤方法是_____________________________。
(4)生产过程中,除NaOH、![]() 可以循环利用外,还可以循环利用的物质有______________(填化学式),用此法制取铝的副产品是_______________(填化学式)。
可以循环利用外,还可以循环利用的物质有______________(填化学式),用此法制取铝的副产品是_______________(填化学式)。
(5)写出![]() 溶液与CaO反应的离子方程式:_________________________。
溶液与CaO反应的离子方程式:_________________________。
(6)若铝土矿中还含有二氧化硅,此生产过程中得到的氧化铝中将混有杂质_______________(填化学式)
【答案】(1)Fe2O3颜料 (2)36 (3)过滤 过滤 向漏斗中加蒸馏水至浸没沉淀,使水自然流完,重复操作2~3次
(4)CaO和CO2Fe2O3和O2
(5)CO32—+CaO+H2O===CaCO3↓+2OH-
(6)SiO2
【解析】
(1)因Al2O3+2NaOH===2NaAlO2+H2O,而Fe2O3不与NaOH溶液发生反应,因此过滤得到的沉淀C为Fe2O3,除利用Fe2O3发生铝热反应制取Fe外,还可作颜料。
(2)2Al2O3(熔融)![]() 4Al+3O2↑,n(O2)=22.4/22.4=1 mol,则m(Al)=4/3mol×27 g/mol=36 g。
4Al+3O2↑,n(O2)=22.4/22.4=1 mol,则m(Al)=4/3mol×27 g/mol=36 g。
(3)操作Ⅰ、Ⅱ、Ⅲ均是除去不溶于液体的固体,即过滤,洗涤方法是向漏斗中加蒸馏水至浸没沉淀,使水自然流完,重复操作2~3次。
(4)据流程图可看出循环使用的物质除NaOH、H2O外,还有CaCO3![]() CaO+CO2↑,CaO与CO2也可循环使用;制取Al同时得到Fe2O3和O2。
CaO+CO2↑,CaO与CO2也可循环使用;制取Al同时得到Fe2O3和O2。
(5)发生的化学反应为Na2CO3+CaO+H2O===CaCO3↓+2NaOH。
(6)据SiO2性质,SiO2+2NaOH===Na2SiO3+H2O,Na2SiO3+CO2+H2O===H2SiO3↓+Na2CO3,H2SiO3![]() SiO2+H2O,因此Al2O3中将混有SiO2。
SiO2+H2O,因此Al2O3中将混有SiO2。