题目内容
(1)相同物质的量的钠、铝、铁与氯气完全作用,消耗氯气的物质的量之比为______. 相同物质的量的钠、铝、铁与盐酸完全反应,恰好全部生成氯化物,则消耗等浓度盐酸的体积之比为______.(2)相同质量的钠、铝、铁与氯气完全作用,消耗氯气的量由大到小的顺序是______;若与盐酸完全反应,恰好全部生成氯化物,则消耗等浓度盐酸的体积由大到小的顺序是______.
【答案】分析:(1)根据反应方程式计算消耗氯气的物质的量以及消耗盐酸的物质的量,进而计算体积;
(2)根据质量计算物质的量,根据反应的方程式计算消耗氯气的物质的量以及消耗盐酸的物质的量,进而计算体积.
解答:解:反应的有关方程式为:2Na+Cl2═2NaCl,2Al+3Cl2═2AlCl3,Fe+3Cl2═FeCl3,
2Na+2HCl═H2↑+2NaCl,2Al+6HCl═3H2↑+2AlCl3,Fe+2HCl═H2↑+FeCl2,
(1)设钠、铝、铁的物质的量分别为1mol,根据反应式可知消耗的氯气的物质的量分别为 mol,
mol, mol,
mol, mol,
mol,
消耗氯气的物质的量之比为: mol:
mol: mol:
mol: mol=1:3:3,
mol=1:3:3,
设钠、铝、铁的物质的量分别为1mol,根据反应式可知消耗的盐酸的物质的量分别为:1mol,3mol,2mol,
消耗盐酸的物质的量之比为:1:3:2,消耗等浓度盐酸的体积之比也为1:3:2,
故答案为:1:3:3;1:3:2;
(2)设钠、铝、铁的质量分别为mg,则钠、铝、铁的物质的量分别为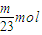 ,
,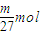 ,
,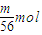 ,
,
根据反应式可知消耗的氯气的物质的量分别为: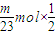 =
=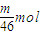 ,
,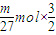 =
=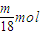 ,
,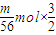 =
=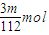 ,
,
消耗氯气的量由大到小的顺序是铝、铁、钠;
根据反应式可知消耗的盐酸的物质的量分别为: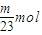 ,
,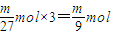 ,
,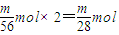 ,
,
消耗盐酸的物质的量的大小顺序为铝、钠、铁,对应的消耗等浓度盐酸的体积由大到小的顺序是铝、钠、铁,
故答案为:铝、铁、钠;铝、钠、铁.
点评:本题考查化学方程式的相关计算,题目难度不大,注意铁与氯气和盐酸反应的不同,为易错点.
(2)根据质量计算物质的量,根据反应的方程式计算消耗氯气的物质的量以及消耗盐酸的物质的量,进而计算体积.
解答:解:反应的有关方程式为:2Na+Cl2═2NaCl,2Al+3Cl2═2AlCl3,Fe+3Cl2═FeCl3,
2Na+2HCl═H2↑+2NaCl,2Al+6HCl═3H2↑+2AlCl3,Fe+2HCl═H2↑+FeCl2,
(1)设钠、铝、铁的物质的量分别为1mol,根据反应式可知消耗的氯气的物质的量分别为
 mol,
mol, mol,
mol, mol,
mol,消耗氯气的物质的量之比为:
 mol:
mol: mol:
mol: mol=1:3:3,
mol=1:3:3,设钠、铝、铁的物质的量分别为1mol,根据反应式可知消耗的盐酸的物质的量分别为:1mol,3mol,2mol,
消耗盐酸的物质的量之比为:1:3:2,消耗等浓度盐酸的体积之比也为1:3:2,
故答案为:1:3:3;1:3:2;
(2)设钠、铝、铁的质量分别为mg,则钠、铝、铁的物质的量分别为
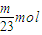 ,
,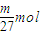 ,
,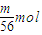 ,
,根据反应式可知消耗的氯气的物质的量分别为:
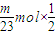 =
=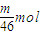 ,
,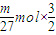 =
=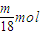 ,
,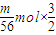 =
=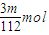 ,
,消耗氯气的量由大到小的顺序是铝、铁、钠;
根据反应式可知消耗的盐酸的物质的量分别为:
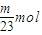 ,
,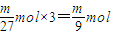 ,
,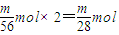 ,
,消耗盐酸的物质的量的大小顺序为铝、钠、铁,对应的消耗等浓度盐酸的体积由大到小的顺序是铝、钠、铁,
故答案为:铝、铁、钠;铝、钠、铁.
点评:本题考查化学方程式的相关计算,题目难度不大,注意铁与氯气和盐酸反应的不同,为易错点.

练习册系列答案
相关题目
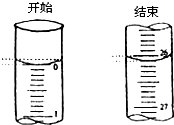 某学生欲用已知物质的量浓度的盐酸来滴定测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:
某学生欲用已知物质的量浓度的盐酸来滴定测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白: