题目内容
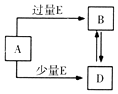
【题目】从固体混合物A出发可以发生如下框图所示的一系列变化.
G为不溶于稀硝酸的白色固体;溶液H的焰色反应呈紫色(透过蓝色的钴玻璃观察).回答下列问题:
(1)在实验室中收集气体C,可选择下图装置中的 . 
(2)操作②的名称是 . 在操作②中所使用的玻璃仪器的名称是 . 在得到固体D时必须进行洗涤、干燥等操作,洗涤固体D的目 .
(3)写出反应①的化学方程式、反应④的离子方程式:反应①: ,
反应④: .
(4)在实验室中,要获得干燥纯净的黄绿色气体F,可以将它通过如图中的装置,其中瓶Ⅰ中盛放的是 , 瓶Ⅱ中盛放的是 .
(5)实验中必须吸收多余的气体F,以免污染空气.下图是实验室用NaOH溶液吸收气体F的装置,为防止产生倒吸现象,合理的装置是 . 
【答案】
(1)AC
(2)过滤;漏斗、玻璃棒、烧杯;除去附着在MnO2表面的K+、Cl﹣等离子
(3)2KClO3 ![]() 2KCl+3O2↑;MnO2+2Cl﹣+4H+═Mn2++Cl2↑+2H2O
2KCl+3O2↑;MnO2+2Cl﹣+4H+═Mn2++Cl2↑+2H2O
(4)饱和食盐水;浓H2SO4
(5)BCD
【解析】解:F为黄绿色气体,则F为Cl2 , 反应④为二氧化锰与浓盐酸的反应,则D为MnO2 , I为MnCl2 , G为不溶于稀硝酸的白色固体;溶液H的焰色反应呈紫色,则G为AgCl,H为KNO3 , E为KCl,混合物B为MnO2、KCl的混合物,则反应①为2KClO3 ![]() 2KCl+3O2↑,A为KClO3、MnO2的混合物,气体C为O2 , (1)氧气不溶于水,可选A用排水法收集,氧气的密度比空气的大,可选C用向上排空气法收集,所以答案是:AC;(2)B为MnO2、KCl的混合物,KCl溶于水,而MnO2不溶于水,可利用过滤来分离,过滤操作使用的玻璃仪器为漏斗、玻璃棒、烧杯,为得到固体D,应利用洗涤除去附着在MnO2表面的K+、Cl﹣等离子,然后再干燥,所以答案是:过滤;漏斗、玻璃棒、烧杯;除去附着在MnO2表面的K+、Cl﹣等离子;(3)反应①的化学方程式为2KClO3
2KCl+3O2↑,A为KClO3、MnO2的混合物,气体C为O2 , (1)氧气不溶于水,可选A用排水法收集,氧气的密度比空气的大,可选C用向上排空气法收集,所以答案是:AC;(2)B为MnO2、KCl的混合物,KCl溶于水,而MnO2不溶于水,可利用过滤来分离,过滤操作使用的玻璃仪器为漏斗、玻璃棒、烧杯,为得到固体D,应利用洗涤除去附着在MnO2表面的K+、Cl﹣等离子,然后再干燥,所以答案是:过滤;漏斗、玻璃棒、烧杯;除去附着在MnO2表面的K+、Cl﹣等离子;(3)反应①的化学方程式为2KClO3 ![]() 2KCl+3O2↑,反应④的离子反应为MnO2+2Cl﹣+4H+═Mn2++Cl2↑+2H2O,所以答案是:2KClO3
2KCl+3O2↑,反应④的离子反应为MnO2+2Cl﹣+4H+═Mn2++Cl2↑+2H2O,所以答案是:2KClO3 ![]() 2KCl+3O2↑;MnO2+2Cl﹣+4H+═Mn2++Cl2↑+2H2O;(4)要获得干燥纯净的黄绿色气体氯气,瓶Ⅰ中盛放饱和食盐水抑制氯气的溶解同时除去混有的HCl,在瓶Ⅱ中盛放浓H2SO4干燥即可,所以答案是:饱和食盐水;浓H2SO4;(5)用NaOH溶液吸收气体氯气的装置,为防止产生倒吸现象,装置中有倒扣的漏斗或肚容式结构,A装置不具有防倒吸的作用,而B、C、D具有,所以答案是:BCD.
2KCl+3O2↑;MnO2+2Cl﹣+4H+═Mn2++Cl2↑+2H2O;(4)要获得干燥纯净的黄绿色气体氯气,瓶Ⅰ中盛放饱和食盐水抑制氯气的溶解同时除去混有的HCl,在瓶Ⅱ中盛放浓H2SO4干燥即可,所以答案是:饱和食盐水;浓H2SO4;(5)用NaOH溶液吸收气体氯气的装置,为防止产生倒吸现象,装置中有倒扣的漏斗或肚容式结构,A装置不具有防倒吸的作用,而B、C、D具有,所以答案是:BCD.
【考点精析】通过灵活运用氯气的实验室制法,掌握实验室制法:MnO2+4HCl(浓)=MnCl2+Cl2↑+2H2O即可以解答此题.

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案