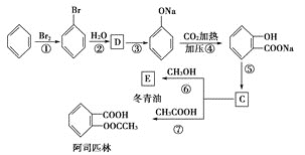
��Ŀ����
����Ŀ������ı����Ϊ5.1��ƽ��������к�������Ϊ3.67��ƽ�����ռ��������������70.8 %��������һ����Ļ�ѧ��Դ���⣬�����Ǻ�ˮ��Դ�ۺ����õIJ�������ͼ������ݸ�ͼ�ش��������⣺
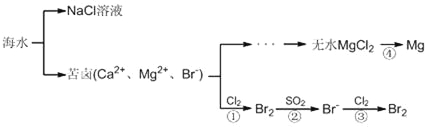
��1��������ˮ�ķ�����__________________��дһ�ֺ����������ɣ����ɺ�ˮ��ȡ�Ĵ����к���Ca2����Mg2����SO42�������ӣ�Ϊ�˳�ȥ��Щ���ӣ���Ҫ���μ����Թ�����NaOH��BaCl2��________���ѧʽ����֮��________����������ƣ����ټ�������________�����Լ����ƣ�����������Һ����Ũ������ȴ�ᾧ���õ����Ρ�
��2����Ӧ������ˮMgCl2��ȡ����þ�ij��ù�ҵ������__________________��
��3�����±��ͨ��Cl2�û���Br2�����ÿ��������岢��SO2���գ�ת��ΪBr����������Σ��Դﵽ�������Ŀ�ġ��ɺ�ˮ��������еķ�Ӧ�ɵó�Cl����SO2��Br����ԭ����ǿ������˳����_________________________��
��4����ҵ��Ҳ������Na2CO3��Һ���մ�����Br2�������廯�ƺ������ƣ�ͬʱ�ų�CO2��д����Ӧ�����ӷ���ʽ__________________________________���������H2SO4����������Һ���µõ�Br2���䷴Ӧ�����ӷ���ʽΪ_______________________________��
���𰸡����� Na2CO3 ���� ���� ��ⷨ SO2��Br����Cl�� 3CO32����3Br2��5Br����BrO3����3CO2�� 5Br����BrO3����6H����3Br2��3H2O
��������
(1)��ˮ��������ʹ��ˮ�еĽ���������Ũ�Ƚ��ͣ��ɲ�������ķ����������������������ȣ���ȥ�����к���Ca2����Mg2����SO42�������ӣ���������������Һ��ȥMg2����������Ca2��������BaCl2��Һ��ȥSO42����Ȼ����Һ�ж����Ba2+��ԭ��Һ�е�Ca2����̼������Һ��ȥ������Ӧ�ټ���Na2CO3��Һ�����˺��ټ���������ϡ�����ȥ��Һ�е�CO32����OH-���ɣ�
��2�����ڽ���Mg�Ļ�Խ�ǿ��ֻ�ܲ��õ��ķ�����ã�ͨ���õ�ⷨ�õ�����þ����3������������ԭ��Ӧ�е������ԡ���ԭ�Ե��жϹ��ɿ�֪��Cl2�û���Br2��˵�������ӵĻ�ԭ�Դ��������ӣ����ÿ��������岢��SO2���գ�ת��ΪBr����˵����������Ļ�ԭ�Դ��������ӣ�����Cl����SO2��Br����ԭ����ǿ������˳����SO2��Br����Cl����
��4����Na2CO3��Һ���մ�����Br2�������廯�ƺ������ƣ�ͬʱ�ų�CO2�����ӷ���ʽΪ3CO32����3Br2��5Br����BrO3����3CO2��������H2SO4����������Һ���µõ�Br2��������������Br����BrO3������������ԭ��Ӧ�����嵥�ʺ�ˮ�����ӷ���ʽΪ5Br����BrO3����6H����3Br2��3H2O��

 �żӾ���ϵ�д�
�żӾ���ϵ�д�����Ŀ����ѧ��Ӧ���ʺ���������������������ء�
��1��ijѧ��Ϊ��̽��п�����ᷴӦ�����е����ʱ仯����400mLϡ�����м���������п�ۣ�����ˮ�������ռ���Ӧ�ų�������(��״��)��ʵ���¼���(�ۼ�ֵ)��
ʱ��(min) | 1 | 2 | 3 | 4 | 5 |
�������(mL) | 100 | 240 | 464 | 576 | 620 |
����һʱ��η�Ӧ�������_______min(��0~1��1~2��2~3��3~4��4~5)����Ӧ��ʼ��Ӧ�����������ԭ����________________��
����3~4����ʱ����������Ũ�ȱ仯����ʾ�ĸ÷�Ӧ����_______(����Һ�������)��
��2����һѧ��Ϊ���Ʒ�Ӧ���ʷ�ֹ��Ӧ�������Բ�������������������������м���������������Һ�Լ�����Ӧ���ʣ�����Ϊ�����е���_______
A������ˮ B��KCl��Һ C��KNO3��Һ D��CuSO4��Һ
��3��ij�¶�����4L�ܱ������У�X��Y��Z������̬���ʵ����ʵ�����ʱ��仯������ͼ
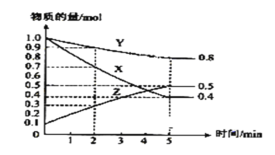
�ٸ÷�Ӧ�Ļ�ѧ����ʽ��____________��
�ڸ÷�Ӧ�ﵽƽ��״̬�ı�־��_________��
A��X��Y��Z�ķ�Ӧ������� B��X��Y�ķ�Ӧ���ʱ�Ϊ3:1
C������������ѹǿ���ֲ��� D������1mol Y��ͬʱ����2mol Z
��2min��X��ת����Ϊ__________��
��ƽ���z��ռ���������Ϊ__________��
����Ŀ������ʵ���С�ʵ�����ݡ�����Ӧ���������ۡ���ϵ����ȷ����
ѡ�� | ʵ������ | ʵ���������� |
A | �ֱ��� 4 mL 0.01 mol/L ��4 mL 0.02 mol/L KMnO4��Һ����2 mL 0.1 mol/L H2C2O4 ��Һ����¼��ɫʱ�� | Ũ��Խ��Ӧ����Խ��Խ����ɫ |
B | ��ʯīΪ�缫����� KI��Һ �����к���������̪�� | �����ݳ������Ҹ�����Һ���ֺ�ɫ |
C | 25��ʱ���� pH=l ������ʹ���� 0.5L����Һ�и����� 1.4g ���� | ����������H2�����ʿ����������� ���� |
D | �� FeCl3+3KSCN | Ѫ��ɫ��dz��˵������������Ũ�ȣ� ƽ�������ƶ� |
A.AB.BC.CD.D
����Ŀ��Ŀǰ�������ƣ�Na2FeO4�����㷺Ӧ����ˮ�Ĵ��������и�Ч�������ŵ㡣ij�غ�ˮ��Ʒ��Na2FeO4�������������Ӽ���Ũ�ȼ��±���H����OH��Ũ��С��δ�г�����
���� | SO42- | Mg2+ | Fe3+ | Na+ | Cl�� |
Ũ��/(mol��L-1) | a | 0.05 | 0.10 | 0.50 | 0.56 |
�����£�ȡһ������Na2FeO4�������ĺ�ˮΪԭ���Ʊ�����ʳ��ˮ��MgCl2��7H2O���������£�
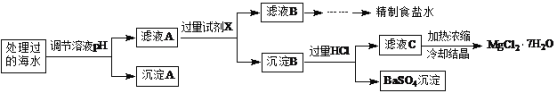
ע�����ӵ�Ũ��С��1.0��10-5 mol��L-1������Ϊ�����Ӳ����ڣ�Ksp[Fe(OH)3]��1.0��10-38��Ksp[Mg(OH)2]��5.0��10-12��������������Һ����ı仯���Բ��ơ�
��1�����ݱ����г�������Ũ�ȼ���a��________������A��_______���ѧʽ����
��2���ڵ�����ҺpHʱ��������Ӧ���ڵ�pH��Χ��_______������Ĺ����Լ�XΪ_______���ѧʽ����
��3���������HCl������Ϊ___________��
��4����Fe��������Cu�����������NaOH��Һ���Ƶ�Na2FeO4����������������ĵ缫��ӦʽΪ___________��