题目内容
6.反应:A2(g)+B2(g)?2AB(g)+Q,当其达到平衡时,改变温度和压强,如图的曲线中,符合勒沙特列原理的是( )
| A. | ①⑤ | B. | ③④ | C. | ① | D. | ①② |
分析 该反应是一个反应前后气体体积不变的放热反应,升高温度,平衡逆向移动,增大压强平衡不移动,据此分析解答.
解答 解:该反应是一个反应前后气体体积不变的放热反应,升高温度,平衡逆向移动,导致AB的含量降低,所以①正确;增大压强平衡不移动,所以AB含量不变,⑤正确,故选A.
点评 本题考查化学平衡移动影响因素,明确温度、压强对化学平衡影响原理是解本题关键,注意该反应特点:放热、反应前后气体体积不变,题目难度不大.

练习册系列答案
相关题目
16.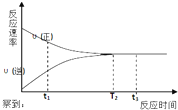 一定条件下的某可逆反应,其正反应速率v(正)和逆反应速率v(逆)随反应时间t的变化如图所示.下列判断不正确的是( )
一定条件下的某可逆反应,其正反应速率v(正)和逆反应速率v(逆)随反应时间t的变化如图所示.下列判断不正确的是( )
 一定条件下的某可逆反应,其正反应速率v(正)和逆反应速率v(逆)随反应时间t的变化如图所示.下列判断不正确的是( )
一定条件下的某可逆反应,其正反应速率v(正)和逆反应速率v(逆)随反应时间t的变化如图所示.下列判断不正确的是( )| A. | t1时刻,v(正)>v(逆) | B. | t2时刻,v(正)=v(逆) | ||
| C. | t2时刻,反应达到最大限度 | D. | t3时刻,反应停止 |
17.下列关于有机化合物的叙述中不正确的是( )
| A. | 丙烷跟甲烷一样能与氯气发生取代反应 | |
| B. | 1 mol乙酸与乙醇在一定条件下发生酯化反应,可生成1 mol乙酸乙酯 | |
| C. | CH2Cl2是纯净物说明甲烷是四面体结构而不是正方形结构 | |
| D. | 溴水既可鉴别乙烷与乙烯,又可除去乙烷中的乙烯而得到纯净的乙烷 |
14.下列溶液中的Cl-浓度与50mL1mol•L一1 MgCl2溶液中的Cl-浓度相等的是( )
| A. | 150 mL 1 mol•L-1NaCl溶液 | B. | 75 mL 2 mol•L-l CaCl2溶液 | ||
| C. | 150 mL 2 mol•L-1KCl溶液 | D. | 75 mL 1 mol•L-1 AlCl3溶液 |
1.下列各组物质中,不管它们以何种比例混合,只要总物质的量一定,充分燃烧后生成的二氧化碳的量和水的量均不变的是( )
| A. | 乙炔和苯 | B. | 乙醇和丙醇 | ||
| C. | 乙醇和乙醚(C2H5OC2H5) | D. | 乙醇和乙烷 |
11.下列化学方程式或离子方程式中,正确的是( )
| A. | 向氢氧化钠溶液中通入少量CO2:CO2+NaOH═NaHCO3 | |
| B. | FeCl3溶液与Cu反应的离子方程式:Fe3++Cu═Cu2++Fe 2+ | |
| C. | 铜与浓硝酸:Cu+4HNO3(浓)═Cu(NO3)2+2NO↑+2H2O | |
| D. | 向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至刚好沉淀完全离子方程式:NH4++H++SO42-+Ba2++2OH-═BaSO4↓+NH3•H2O+H2O |
18.下列分子和离子中,中心原子价层电子对的几何构型为四面体且分子或离子的空间构型为V形的是( )
| A. | OF2 | B. | SO2 | C. | H3O+ | D. | NH${\;}_{4}^{+}$ |
16.下列试剂的贮存方法错误的是( )
| A. | 苯用带橡胶塞的试剂瓶贮存 | B. | 浓硝酸存放在棕色试剂瓶中 | ||
| C. | 少量白磷存放在水中 | D. | 少量金属钠存放在煤油中 |
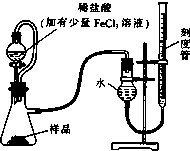 过氧化镁(MgO2)易溶于稀酸,溶于酸后产生过氧化氢,在医学上可作为解酸剂等.过氧化镁产品中常会混有少量MgO,实验室可通过多种方案测定样品中过氧化镁的含量.
过氧化镁(MgO2)易溶于稀酸,溶于酸后产生过氧化氢,在医学上可作为解酸剂等.过氧化镁产品中常会混有少量MgO,实验室可通过多种方案测定样品中过氧化镁的含量.