题目内容
【题目】下列关于各图象的解释或得出结论正确的是( )


A. 图甲表示0.10molL﹣1NaOH溶液滴定20.00 mL 0.10 molL﹣1醋酸溶液的滴定曲线
B. 图乙表示向乙酸溶液中通入氨气至过量过程中溶液导电性I的变化
C. 根据图丙所示可知:石墨转化为金刚石吸收热量,石墨比金刚石稳定
D. 图丁表示反应2SO2+O22SO3,t1时刻只减小了 SO3的浓度
【答案】C
【解析】醋酸是弱酸,所以0.10mol/L的醋酸的pH一定大于1,但是图像的起点pH为1,所以选项A错误。乙酸和氨气反应得到乙酸铵,将乙酸这样的弱电解质转化为乙酸铵这样的强电解质,所以溶液的导电性应该增强,选项B错误。图丙明显得到金刚石能量更高,所以石墨转化为金刚石吸收热量,石墨比金刚石稳定,选项C正确。图丁的t1时刻如果只减少了 SO3的浓度,图像为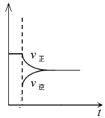 ,所以选项D错误。
,所以选项D错误。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目