题目内容
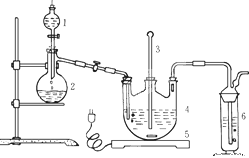
【题目】将含有C,H,O的有机物3.24g装入元素分析装置,通入足量的O2使之完全燃烧,将生成的气体依次通过CaCl2管(A)和碱石灰(B),测得A管质量增加了2.16g,B管增加了9.24g,已知该有机物的相对分子质量为108.
(1)燃烧此有机物3.24g需消耗O2多少g?
(2)求此有机物的分子式.
【答案】
(1)O28.16g
(2)C7H8O
【解析】解:(1)化学反应遵循质量守恒定律,则消耗O2的质量为:2.16+9.24﹣3.24=8.16g,
答:燃烧此有机物3.24g需消耗O28.16g.(2)CaCl2中吸水质量增加2.16g,即生成水 ![]() =0.12mol,含H0.24mol,
=0.12mol,含H0.24mol,
碱石灰吸CO2增加9.24g,即生成 ![]() =0.21mol,
=0.21mol,
该有机物物质的量为 ![]() =0.03mol,
=0.03mol,
所以含C: ![]() =7,
=7,
含H: ![]() =8,
=8,
根据相对分子质量判断,还应含O: ![]() =1,
=1,
所以有机物的分子式为:C7H8O,
答:有机物的分子式为C7H8O.

【题目】研究物质的微观结构,有助于人们理解物质变化的本质。
(1)N、Al、Si、Zn四种元素中,有一种元素的电离能数据如下:
电离能 | I1 | I2 | I3 | I4 | I5 | …… |
Im/kJ·mol-1 | 578 | 1817 | 2745 | 11575 | 14830 | …… |
则该元素是______(填元素符号)。
(2)氮元素可以形成许多化合物,在我们生活生产中有广泛的应用。
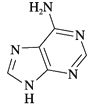
①维生素B4结构如图所示,则碳原子的轨道杂化类型是_________;1 mol维生素B4分子中含有σ键的数目为________。
②NF3的空间构型为______(用文字描述);与NF3分子互为等电子体的阴离子为______(填化学式)。
(3)过渡元素常与H2O、NH3、CN-、SCN-等形成配合物。
①C、N、O三种元素的电负性由大到小的顺序为________。
②X、Y均为第四周期元素。X基态原子的内层轨道全部排满电子,且最外层电子数为1。Y基态原子在同周期元素中未成对电子数最多,则X+基态核外电子排布式________;元素Y在周期表中位于第________族。
③在配离子[Fe(SCN)]2+中,提供空轨道的是________;[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,则[Zn(CN)4]2-的结构可用示意图表示为________。