��Ŀ����
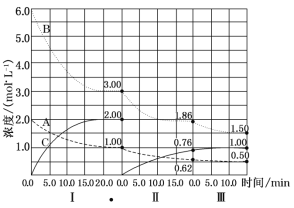
����Ŀ�������£���1��000mol/L�������20��00mL1��000mol/L��ˮ�У���ҺpH���¶��������������仯��������ͼ��ʾ�������й�˵����ȷ����

A. a����ˮ�������c��H������1��0��10��14mol/L
B. b��ʱc��NH4������c��NH3��H2O����c��Cl����
C. c��ʱ���ĵ����������V��HCl��<20��00mL
D. d�����Һ�¶����½�����Ҫԭ����NH3��H2O��������
���𰸡�C
�����������������A����a��7��pH��14�����ˮ�������c��H+����1��0��10-14molL-1��A����B������Ͱ�ˮ��Ӧ����Һ�����ԣ���c��H+��=c��OH-�������ݵ���غ��֪c��Cl-��=c��NH4+����b��ʱpH��7����ˮ������c��NH4+��+c��NH3H2O����c��Cl-����B����C��C����Һ�����ԣ���c��H+��=c��OH-�����Ȼ����ǿ�������Σ���ˮ��Һ�����ԣ�Ҫʹ��ˮ��Һ�����ԣ���ˮӦ��������������������������V��HCl����20��00mL��C��ȷ��D��d��ʱ����Ͱ�ˮǡ����ȫ��Ӧ��������࣬�ټ������¶Ƚ���ֻ���Ǽ���������¶ȵ�����Һ�¶ȣ�������¶��½���ԭ��D����ѡC��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�