题目内容
在等物质的量浓度的两种弱酸的钠盐(NaR、NaR′)溶液中分别通入适量的CO2,发生如下反应:NaR+CO2+H2O====HR+NaHCO3,2NaR′+CO2+H2O====2HR′+ Na2CO3,把HR和HR′在水中电离出H+的能力作比较,正确的判断是( )
| A.HR较强 | B.HR′较强 | C.两者相同 | D.无法比较 |
A
此题实际比较HR和HR′酸性强弱。由强酸制弱酸原理,依题意知酸性大小关系为:HR>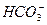 >HR′。
>HR′。
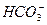 >HR′。
>HR′。
练习册系列答案
 期末集结号系列答案
期末集结号系列答案
相关题目
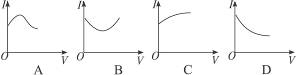
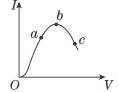
 NH4++OH—,下列叙述正确的是:( )
NH4++OH—,下列叙述正确的是:( )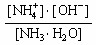 。氨水中各离子和分子的浓度大小关系为( )
。氨水中各离子和分子的浓度大小关系为( )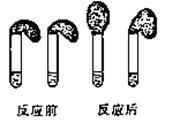
 l溶液各100mL;
l溶液各100mL;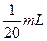 )分别稀释至100mL,
)分别稀释至100mL, ·L-1H2SO4 D.2mol·L-1HA
·L-1H2SO4 D.2mol·L-1HA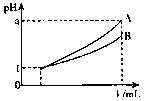
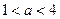 ,则A、B都是弱酸
,则A、B都是弱酸