题目内容
下列有关化学用语表示正确的是( )
| A.漂白粉有效成分的化学式:CaClO |
B.Na+的结构示意图: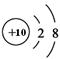 |
C.原子核内有10个中子的氧原子: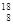 O O |
| D.NaHCO3在水溶液中的电离方程式:NaHCO3=Na++H++CO32— |
C
解析试题解析:A、漂白粉的有效成分的化学式应为Ca(ClO)2,错误;B、Na+的原子核内应有11个质子,错误;C、818O原子核内有10个中子,正确;D、NaHCO3在水溶液中的电离方程式应为:NaHCO3=Na++HCO3-,错误,答案选C。
考点:考查化学术语有关知识的运用

练习册系列答案
相关题目
用98%的浓硫酸(密度1.84g · mL-1)配制100mL 1mol·L-1的稀硫酸。现给出下列配制中可能用到的仪器:①100 mL量筒;②10 mL量筒;③50 mL烧杯;④托盘天平;⑤100 mL容量瓶;⑥胶头滴管;⑦玻璃棒。按使用仪器的先后顺序作出的下列排列中正确的是
| A.④③⑥⑦⑤⑥ | B.②⑥③⑦⑤⑥ | C.①③⑤⑦⑤⑥ | D.②③⑥⑦⑤⑥ |
下列叙述正确的是(NA为阿伏加德罗常数的值)
| A.1 mol Na2O·SiO2中含有NA个Na2O |
| B.在H2O2+Cl2=2HCl+O2反应中,每生成32 g氧气,则转移NA个电子 |
| C.标准状况下,分子数为NA的CO、C2H4混合气体体积约22.4 L,质量为28 g |
| D.4.6 g Na与适量氧气完全反应生成Na2O、Na2O2的混合物中含有的阴离子数大于0.1NA |
用NA表示阿伏加德罗常数的值,则下列叙述正确的是( )
| A.1 mol过氧化钡(BaO2)晶体中所含有的阴离子数目为2NA |
| B.标准状况下,22.4 L四氯化碳中所含有的共价键数目为4NA |
| C.将1 mol FeCl3转化为氢氧化铁胶体,得到的氢氧化铁胶体粒子数小于NA |
| D.常温常压下,33.6 L氯气与56 g铁充分反应,转移的电子数为3NA |
下列有关化学用语表示正确的是( )。
| A.二氧化硅的分子式:SiO2 |
| B.聚乙烯的结构简式:?CH2CH2? |
| C.高氯酸钠(NaClO4)中Cl元素的化合价:+6 |
| D.Mg5(Si4O10)2(OH)2·4H2O的氧化物形式:5MgO·8SiO2·5H2O |
用NA表示阿伏加德罗常数的值。下列叙述中正确的是 ( )。
| A.7.8 g Na2O2中含有的阴离子数为0.2NA |
| B.铜与浓硫酸反应中,当转移的电子数为0.2NA时,生成的SO2为2.24 L |
| C.1 mol·L-1的NH4Cl溶液中的NH4+的数目小于NA |
| D.由NO2、O2组成的混合物中共有NA个分子,其中的氧原子数目为2NA |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )。
| A.常温下,4 g CH4含有NA个C—H共价键 |
| B.1 mol Fe 与足量的稀HNO3反应,转移2NA个电子 |
| C.1 L 0.1 mol·L-1 NaHCO3溶液中含有0.1NA个HCO3— |
| D.常温常压下,22.4 L的NO2和CO2混合气体含有2NA个O原子 |
下列叙述正确的是( )
| A.1.00 mol NaCl中含有6.02×1023个NaCl分子 |
| B.1.00 mol NaCl中,所有Na+的最外层电子总数为8×6.02×1023 |
| C.欲配制1.00 L 1.00 mol·L-1的NaCl溶液,可将58.5 g NaCl溶于1.00 L水中 |
| D.电解58.5 g熔融的NaCl,能产生22.4 L氯气(标准状况)、23.0 g金属钠 |
 KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6NA
KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6NA