题目内容
氢气还原氧化铜所得的红色固体可能是铜与氧化亚铜的混合物,已知Cu2O在酸性溶液中可发生自身氧化还原反应,生成Cu2+和Cu。
(1)现有8.4克氧化铜被氢气完全还原后,得到红色固体6.96克,其中含单质铜与氧化亚铜的物质的量之比是 ;
(2)若将6.96克上述混合物与足量的浓硝酸充分反应:
①生成标准状况下1.568升的气体(不考虑NO2的溶解,也不考虑NO2与N2O4的转化),则该气体的成分是 ,其物质的量之比是 ;
②把得到的溶液小心蒸发浓缩,把析出的晶体过滤,得晶体20.328g。经分析,原溶液中的Cu2+有20%残留在母液中,所得晶体的化学式为 。
(3)Cu、Cu2O和CuO组成的混合物,加入100mL 0.6mol/L HNO3溶液恰好使混合物完全溶解,同时收集到224mL NO气体(标准状况)。如原混合物中Cu的物质的量为X,求其中Cu2O、CuO的物质的量及X的取值范围(写出解题过程)。
(1)现有8.4克氧化铜被氢气完全还原后,得到红色固体6.96克,其中含单质铜与氧化亚铜的物质的量之比是 ;
(2)若将6.96克上述混合物与足量的浓硝酸充分反应:
①生成标准状况下1.568升的气体(不考虑NO2的溶解,也不考虑NO2与N2O4的转化),则该气体的成分是 ,其物质的量之比是 ;
②把得到的溶液小心蒸发浓缩,把析出的晶体过滤,得晶体20.328g。经分析,原溶液中的Cu2+有20%残留在母液中,所得晶体的化学式为 。
(3)Cu、Cu2O和CuO组成的混合物,加入100mL 0.6mol/L HNO3溶液恰好使混合物完全溶解,同时收集到224mL NO气体(标准状况)。如原混合物中Cu的物质的量为X,求其中Cu2O、CuO的物质的量及X的取值范围(写出解题过程)。
(1)5∶1
(2)①NO、NO2,(1分) 11∶3 (2分)
②Cu(NO3)2·3H2O(2分)
(3)n(Cu2O)=(0.015-x) mol (2分)
n(CuO)= (x-0.005) mol(2分) 0.005<x<0.015 (1分)
(2)①NO、NO2,(1分) 11∶3 (2分)
②Cu(NO3)2·3H2O(2分)
(3)n(Cu2O)=(0.015-x) mol (2分)
n(CuO)= (x-0.005) mol(2分) 0.005<x<0.015 (1分)
试题分析:(1)设单质铜与氧化亚铜的物质的量分别为x和y,则根据铜原子守恒可知x+2y=
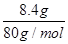 =0.105mol。又因为64g/mol×x+144g/mol×y=6.96g,解得x=0.075mol、y=0.015mol,因此单质铜与氧化亚铜的物质的量之比为5∶1。
=0.105mol。又因为64g/mol×x+144g/mol×y=6.96g,解得x=0.075mol、y=0.015mol,因此单质铜与氧化亚铜的物质的量之比为5∶1。(2)①反应中转移电子的物质的量为0.075mol×2+0.015mol×2×1=0.18mol,气体的物质的量是1.568L÷22.4L/mol=0.07mol。设混合气中NO和NO2的物质的量分别为a mol和b mol,则a+b=0.07、3a+b=0.18,解得a=0.055mol、b=0.015mol,因此混合气的成分是NO和NO2,其体积之比为11∶3。
②设晶体的化学式为Cu(NO3)2·nH2O,则根据铜离子守恒可知晶体中铜离子的物质的量为0.105mol×80%=0.084mol,因此晶体的物质的量也是0.084mol,则0.084mol×(192+18n)g/mol=20.328g,解得n=3,即晶体化学式为Cu(NO3)2·3H2O。
(3)设Cu2O、CuO的物质的量分别为Ymol、Zmol,则根据铜原子守恒可知生成硝酸铜的物质的量为(X+2Y+Z)mol。NO的物质的量是0.01mol,则根据电子得失守恒可知2X+2Y=0.01×3=0.03。硝酸的物质的量是0.06mol,则根据氮原子守恒可知2×(X+2Y+Z)+0.01=0.06,解得Z=(x-0.005),Y=(0.015-x)。由于Y、Z均不能为0,作为X的取值范围是0.005<x<0.015。

练习册系列答案
相关题目
 +O2+xOH-===Fe3O4+S4O
+O2+xOH-===Fe3O4+S4O +2H2O,下列说法中,正确的是( )
+2H2O,下列说法中,正确的是( )
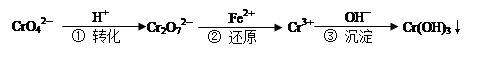
 Fe(OH) 2↓+ 2H+
Fe(OH) 2↓+ 2H+