题目内容
取x g铜镁合金完全溶于浓硝酸中,反应过程中硝酸被还原只产生8 960 mL的NO2气体和672 mL N2O4的气体(都已折算到标准状态),在反应后的溶液中加足量的氢氧化钠溶液,生成沉淀质量为17.02 g。则x等于( )
| A.8.64 g | B.9.20 g |
| C.9.00 g | D.9.44 g |
B
铜镁合金的质量等于沉淀质量减去OH-的质量,n(OH-)=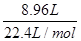 ×1+
×1+ ×2=0.46 mol,其质量为0.46 mol×17 g·mol-1=7.82 g
×2=0.46 mol,其质量为0.46 mol×17 g·mol-1=7.82 g
铜镁合金质量为17.02 g-7.82 g=9.20 g,B正确。
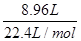 ×1+
×1+ ×2=0.46 mol,其质量为0.46 mol×17 g·mol-1=7.82 g
×2=0.46 mol,其质量为0.46 mol×17 g·mol-1=7.82 g铜镁合金质量为17.02 g-7.82 g=9.20 g,B正确。

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目




 Cu2++Cu。根据以上信息,结合自己所掌握的化学知识,回答:
Cu2++Cu。根据以上信息,结合自己所掌握的化学知识,回答: